
| A. | 铝片与稀H2SO4反应 | B. | 灼热的炭与H2O反应 | ||
| C. | Ba(OH)2•8H2O与NH4Cl反应 | D. | 甲烷在O2中的燃烧反应 |
科目:高中化学 来源: 题型:解答题
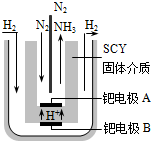 合成氨工业及硝酸工业对工、农生产和国防都有重要意义.请回答:
合成氨工业及硝酸工业对工、农生产和国防都有重要意义.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
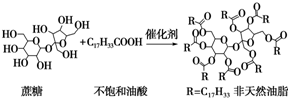
| A. | 蔗糖酯属于油脂类物质 | |
| B. | 该非天然油脂为高分子化合物 | |
| C. | 该非天然油脂与氢氧化钠溶液共热,其水解产物不与溴水反应 | |
| D. | 该蔗糖酯在稀硫酸的作用下水解,最终可生成三种有机化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
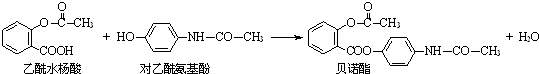
| A. | 贝诺酯分子中只有一种官能团 | |
| B. | 两种反应物均能与NaHCO3溶液反应放出CO2 | |
| C. | 可用FeCl3溶液区别乙酰水杨酸和对乙酰氨基酚 | |
| D. | 贝诺酯与足量NaOH溶液共热,生成三种羧酸盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4•14H2O | B. | CH4•8H2O | C. | CH4•($\frac{23}{3}$)H2O | D. | CH4•6H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的燃烧热为△H=-890.3kJ•mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | 已知H2O(l)═H2O(g)△H=+44 kJ•mol-1,则2gH2(g)完全燃烧生成液态水比生成气态水多释放22kJ的能量 | |
| C. | 吸热反应一定是非自发的化学反应 | |
| D. | 同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
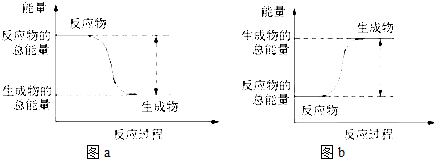
| A. | 图a表示的是吸热反应的能量变化 | |
| B. | 图b中反应物比生成物稳定 | |
| C. | 图b可以表示氯化铵固体与氢氧化钡晶体反应的能量变化 | |
| D. | 图a不需要加热就一定能发生,图b一定需要加热才能发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯(苯酚):溴水,过滤 | |
| B. | 乙酸乙酯(乙酸):乙醇及浓硫酸,加热蒸馏 | |
| C. | 乙醇(水):无水氯化钙,分液 | |
| D. | 乙炔(H2S、PH3):硫酸铜溶液,洗气 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,雷电作用能进行氮的固定,写出反应方程式N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO.
,雷电作用能进行氮的固定,写出反应方程式N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com