

| A. | 溶液中一定存在Mg2+和SO42- | |
| B. | 一定不存在Fe2+、Ba2+和CO32- | |
| C. | Cl-可能存在 | |
| D. | 必须通过焰色反应来确定溶液中是否存在K+ |
分析 加入硝酸银生成白色沉淀,可能生成氯化银或硫酸银或二者都有;
加入氢氧化钠溶液,且露置在空气中生成0.58g白色沉淀,可不含Fe2+,一定含有Mg2+,且n(Mg2+)=$\frac{0.58g}{58g/mol}$=0.01mol,则不含CO32-;
加入足量的氯化钡溶液生成4.66g白色沉淀,说明含有SO42-,且n(SO42-)=$\frac{4.66g}{233g/mol}$=0.02mol,则一定不含Ba2+,结合溶液的电中性确定是否含有钾离子,以此解答该题.
解答 解:A.由以上分析可知溶液中一定存在Mg2+和SO42-,故A正确;
B.由以上分析可知一定不存在Fe2+、Ba2+和CO32-,故B正确;
C.因含有硫酸根离子,可生成硫酸银沉淀,不能确定氯离子,故C正确;
D.n(SO42-)=$\frac{4.66g}{233g/mol}$=0.02mol,n(Mg2+)=$\frac{0.58g}{58g/mol}$=0.01mol,由溶液的电荷守恒可知一定含有钾离子,故D错误.
故选D.
点评 本题考查无机物的推断,涉及物质检验实验方案的设计,为高频考点,把握实验中发生的反应、现象与结论的关系为解答的关键,侧重分析与实验能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,任何气体的摩尔体积都是22.4L | |
| B. | 11.2LCO2中含11NA个电子 | |
| C. | 标况下,NA个水分子所占的体积约为22.4L | |
| D. | 4℃时,18mL水和32gO2所含分子数均为1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 制备Al(OH)3悬浊液:向1mol•L-1AlCl3溶液中滴加过量的6mol•L-1氨水 | |
| B. | 提纯含有少量苯酚的苯:向含有少量苯酚的苯中加入适量浓溴水,过滤 | |
| C. | 检验溶液中是否含有Fe2+:取少量待检验溶液,向其中加入少量新制氯水,再滴加KSCN溶液,观察实验现象 | |
| D. | 探究催化剂对H2O2分解速率的影响:在相同条件下,向一支试管中加入2mL5%H2O2和1mLH2O,向另一支试管中加入2mL5%H2O2和1mLFeCl3溶液,观察并比较实验现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
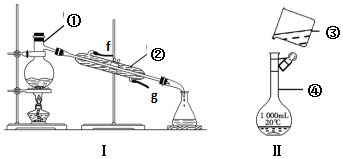
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验目的 | 实验操作 | |
| A | 证明溶液中一定含有SO32- | 将该溶液与稀盐酸反应产生的气体通入澄清石灰水,有白色沉淀生成 |
| B | 证明氯气中混有氯化氢气体 | 将该混合气体通入AgNO3溶液中,有白色沉淀生成 |
| C | 证明某固体中有Na+,无K+ | 灼烧该固体,火焰呈黄色 |
| D | 证明Br-还原性强于Cl- | 向NaBr溶液中滴入少量氯水和苯,振荡、静置,溶液上层呈橙红色 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4LH2O含有分子数为1NA | |
| B. | 常温常压下,224LH2和O2的混合气体所含分子数为NA | |
| C. | 通常状况下,1molCl2与足量Na反应转移电子数为NA | |
| D. | 常温下,2.7g铝与足量的盐酸反应,失去的电子数为0.3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 性质 | 实际应用 |
| A | 氧化铝的熔点高 | 作耐火材料 |
| B | 铁比铜金属活动性强 | 氯化铁溶液腐蚀铜刻制印刷电路板 |
| C | 硅胶多孔,吸水强 | 作袋装食品的干燥剂 |
| D | 金属化合物灼烧有特殊颜色 | 作节日燃放的烟花 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com