
����Ŀ����ͼ����MgCl2��AlCl3�����Һ������ʼ�μ�7 mL�Լ�A��֮��ĵμ��Լ�B�����ó������ʵ���y (mol) ���Լ����V(mL)��Ĺ�ϵ��ͼ��ʾ��(�Լ�A��B�ֱ���NaOH ��Һ�����е�һ��)
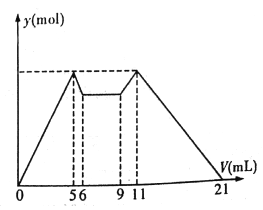
���½��۲���ȷ����
A. A��NaOH ��Һ��B������
B. ԭ���Һ����c(Al3+) :c(Mg2+) :c(Cl-)=1:1:5
C. c(NaOH) :c(HCl)=1:2
D. ��6 ��9 �Ĺ������������ķ�Ӧ�����ӷ�Ӧ����ʽ��H+ +OH-=H2O
���𰸡�C
������������ͼ��֪��MgCl2��AlCl3�����Һ�У���ʼ�μ�7mL�Լ�A������A��������������NaOH��MgCl2��AlCl3��Ӧ���ɳ�����HCl����Ӧ������A��NaOH��B��HCl��5mL��11mLʱ���������������ȣ�ΪAl(OH)3��Mg(OH)2�������������ֳ�������5mLNaOH��������ȫ�ܽ�����10mLHCl���൱����Ӧ�������1��1��Ӧ���������֮��Ϊ1��2����c(NaOH)��c(HCl)=2��1��5-6mLʱ��NaOH�ܽ�������������������1mL������������������������NaOH���Ӧ����3mL��0-5mLΪ����Al(OH)3��Mg(OH)2����������2mLΪ����Mg(OH)2����ʱ���ĵ�����������Һ����������Al(OH)3��Mg(OH)2��������NaOH����ֱ���3mL��2mL�����ݹ�ϵʽ֪��c(Al3+)��c(Mg2+)=1��1��A.��������������A��NaOH��Һ��B�����ᣬ��A��ȷ��B���Ӽ���5 mL A���ɳ�����࣬�ټ�����1 mL A���������ٵ���Сֵ����Ӧ��Ӧ�����ӷ���ʽΪ��Al(OH)3+OH-=AlO2-+2H2O���ɴ˿�֪��n(Al3+)=n��Al(OH)3��=(1��6��10-3) mol����ǰ5 mL NaOH�γ�����������֪��2n(Mg2+)+3n(Al3+)=(5��10-3��6)mol������n(Mg2+)=(1��6��10-3) mol����Һ�������������������ȵã�n(Cl-)=(5��10-3��6)mol������Һ��c(Mg2+)��c(Al3+)��c(Cl-)=1��1��5����B��ȷ��C�����ݼ���ǰ6 mL�Լ�ʱ�����г������ɶ����ܽ⣬���ԣ��Լ�A��NaOH����B�����ᣬ����ͼ��֪��0��5(5 mL)��11��21(10mL)�ֱ��ǵõ�Al(OH)3��Mg(OH)2�����ͳ����ܽ⣬���������൱����Ӧ�������1��1��Ӧ���������֮��Ϊ1��2����c(NaOH)��c(HCl)=2��1����C����D����6mL��9mL��ӦҺ���г�������ȣ�������֪��ʱ������������кͷ�Ӧ����H++OH-=H2O����D��ȷ����ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�������һ���ܴ���������ǣ� ��
A. ����ɫ��Һ�У�Na+ Fe3+ Cl�� SO42-
B. �ں�����Fe3+ ����Һ�У�NH4+ K+ NO3- OH��
C. ��ǿ����Һ�У�Na+ K+ NO3- CO32��
D. �μ���ɫʯ���Լ��Ժ����Һ�У�K+ Fe2+ Cl�� CO32��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���ӷ�Ӧ�漰��H2O��ClO����NH4+��OH����N2��Cl������������N2��ClO�������ʵ�����ʱ��仯��������ͼ��ʾ������˵����ȷ���ǣ� �� 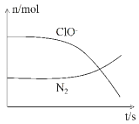
A.�÷�Ӧ��Cl��Ϊ��������
B.����1 mol��ԭ����ת��6 mol����
C.��Ӧ����Һ�����Լ���
D.NH4+��ClO��������N2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���ԣ� ![]() ��H2CO3��
��H2CO3�� ![]() ���ۺϿ��Ƿ�Ӧ���ת���ʺ�ԭ�ϳɱ������أ���
���ۺϿ��Ƿ�Ӧ���ת���ʺ�ԭ�ϳɱ������أ��� 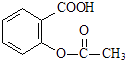 ת��Ϊ
ת��Ϊ 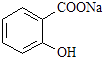 ����ѷ����ǣ� ��
����ѷ����ǣ� ��
A.��ϡH2SO4���Ⱥ���������NaOH��Һ
B.��ϡH2SO4���Ⱥ���������NaHCO3��Һ
C.��������NaOH��Һ���Ⱥ���ͨ������CO2
D.��������NaOH��Һ���Ⱥ��ټ�������H2SO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о��绯ѧ��ʴ��������װ����ͼ��ʾ�������й�˵����ȷ���ǣ� �� 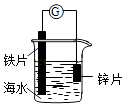
A.пƬ����������Ӧ������
B.���Ӵ���Ƭ������������пƬ
C.��Ƭ�ϵ缫��ӦΪ��O2+2H2O+4e��4OH��
D.��װ�ÿ������о���ӵ�������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����CuO��Zn�۵Ļ�����У�����һ������ϡ���ᣬ���ȣ�����Ӧֹͣ���˳������������Һ�в���һöпƬ������пƬ�����κα仯��������������ȷ�����������ȷ����
A. ������һ����Cu B. ������һ����Cu������һ����Zn
C. ������һ����Zn D. ��Һ��һ������Zn2��������һ������Cu2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС�����ⶨij�Ѳ��ֱ��ʵ�С�մ���Ʒ��Na2CO3�������������������ʵ�鷽����
������һ����ȡһ��������Ʒ�����������м��������غ�����ȴ������ʣ��������������㡣
��1�������з�����Ӧ�Ļ�ѧ����ʽΪ_______________��
��2��ʵ���У�����������ص�Ŀ����_______________��
������������ȡһ��������Ʒ������С�ձ��У�������ˮ�ܽ�����С�ձ��м�������Ba(OH)2��Һ��������ϴ�ӡ���������������������������㡣(��֪:Ba2++OH-+HCO3-==BaCO3��+H2O)
��1�����˲������������ձ���©��������Ҫ�õ��IJ�������Ϊ_______________��
��3��ʵ�����жϳ����Ƿ���ȫ�ķ�����_______________��
����������������ͼ��ʾװ�ý���ʵ��:
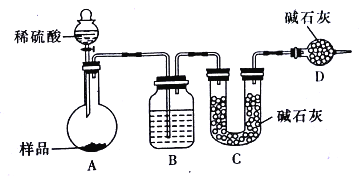
��1��Dװ�õ�������_______________����Һ©����_________(������������������)���������ϡ�������ʵ�顣
��2��ʵ��ǰ��ȡ17.90g��Ʒ��ʵ�����Cװ������8.80g������Ʒ��Na2CO3����������Ϊ________________(������λ��Ч����)
��3�����ݴ�ʵ���õ����ݣ��ⶨ������������Ϊʵ��װ�û������һ������ȱ����________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ʵ���Ҫ���Ԫ��֮һ���������������������������أ�
��1����ԭ�����������Ų�ʽΪ���������ӣ�N3�������������˶�״̬��ͬ�ĵ��ӣ�N4���ӵĿռ�ṹ��ͼ�� ![]() ������һ�����ӣ�������ԡ��Ǽ��ԡ���
������һ�����ӣ�������ԡ��Ǽ��ԡ���
��2���������˹��̵��IJ������������ˮ��1��700��������NH3H2O�������ʵ��֤��NH3H2O������ ��
��3����100mL 0.1mol/L��������ͨ��0.02mol������������պ�����Һ�ʼ��ԣ������Һ��NH3H2O��NH4+��Cl�������������ʵ���Ũ�ȴ�С��ϵΪ ��
��4����ο��������ʣ�ʵ���Ҽ�������е�NH4+ʱ����ȡ���������Ʒ���Թ��У�����ǿ��Ũ��Һ�����ȣ���������������ʹ �� ˵����NH4+ ��
��5��NaN3����������������ȫ���ң�����������ײ��ʱ��NaN3��Ѹ�ٷֽ����Na��N2 �� ��д���÷�Ӧ�Ļ�ѧ����ʽ �� ÿ����3mol N2ʱ��ת�Ƶ���mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B�����л�����ɵĻ����������������һ��ʱ������A��B�Ժ��ֱ�����ϣ���ȫȼ�պ�����CO2������Ϊ��ֵ���������һ�������л�������ǣ� ��
A.�״���CH3OH�����Ҷ�����HOCH2CH2OH��
B.��ȩ��HCHO������ȩ ��CH3CHO��
C.CH4�� 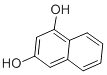
D.����C6H6���ͱ��ӣ�C6H5OH��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com