
| A、AgNO3[AgNO3] |
| B、NaOH[H2O] |
| C、KCl[KCl] |
| D、CuSO4[Cu(OH)2] |


 一线名师提优试卷系列答案
一线名师提优试卷系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
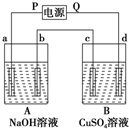 用惰性电极按如图中装置完成实验,其中A、B两烧杯分别盛放200g 10% NaOH溶液和足量CuSO4溶液.通电一段时间后,c极上有Cu析出,又测得A杯溶液中NaOH的质量分数为10.23%,试回答:
用惰性电极按如图中装置完成实验,其中A、B两烧杯分别盛放200g 10% NaOH溶液和足量CuSO4溶液.通电一段时间后,c极上有Cu析出,又测得A杯溶液中NaOH的质量分数为10.23%,试回答:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该反应既属于四种基本类型的反应,又属于氧化还原反应 |
| B、氧元素被还原,硫元素被氧化 |
| C、每有3 mol S参加反应转移6 mol电子 |
| D、S既是氧化剂又是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、62 g Na2O与78gNa2O2中所含阴离子的个数比为1:2 |
| B、质量相等的两份气体,一份是SO2,另一份是SO3,这两份气体中,SO2与SO3所含氧原子个数之比是6:5 |
| C、在标准状况下,0.5NA个水分子所占体积是11.2 L |
| D、500 mL 1 mol/L Fe2(SO4)3溶液,同250 mL 3 mol/L的Na2SO4溶液所含硫酸根离子的物质的量浓度之比为1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、能使甲基橙变红的溶液:NH4+、Na+、SO42-、Fe3+ |
| B、无色澄清溶液:K+、HCO3-、SO42-、Al3+ |
| C、与金属铝反应能放出氢气的溶液:NH4+、NO3-、SO42-、Na+ |
| D、水电离产生的c(H+)=1×10-12mol/L的溶液:HCO3-、NH4+、Cl-、Ca2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
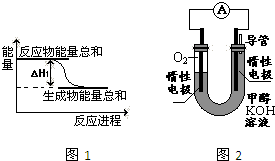 甲醇是一种可再生能源,具有广泛的开发和应用前景.
甲醇是一种可再生能源,具有广泛的开发和应用前景.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com