
| A. | 杜绝铝制品在生产生活中的应用 | |
| B. | 不能用铝制器皿长期存放酸性或碱性食品 | |
| C. | 不吃或少吃使用了含铝食品添加剂的食物 | |
| D. | 氢氧化铝可用于药物治疗胃酸过多 |
分析 A.作为金属材料,铝的优良性能比较多,比如导电性好、导热率高、轻便易加工等;
B.无论是铝还是其氧化物都能与酸或碱反应;
C.铝在生物体内长期积累会对神经系统等造成危害;
D.氢氧化铝没有腐蚀性,能与盐酸反应.
解答 解:A.作为金属材料,铝的优良性能比较多,比如导电性好、导热率高、轻便易加工等,铝在生产生活中应用广泛,不能因其缺点而否定其优点,故A错误;
B.无论是铝还是其氧化物都能与酸或碱反应,不能用铝制器皿长期存放酸性或碱性食品,故B正确;
C.不吃或少吃使用了含为铝食品添加剂的食物,铝在生物体内长期积累会对神经系统等造成危害,故C正确;
D.氢氧化铝没有腐蚀性,能与盐酸反应,所以氢氧化铝可用于药物治疗胃酸过多,故D正确.
故选A.
点评 本题考查了铝的性质分析判断,铝的性质与人体健康,“关爱生命,拥抱健康”是人类追求的永恒主题,对营养元素与人体健康的考查也就成了热点之一,特别是元素的分类、元素的生理功能和对人体的影响等内容,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 分离Al2O3与Fe2O3混合物可以采取加入过量NaOH溶液充分反应后,过滤、洗涤、干燥 | |
| B. | 用过量氨水除去Fe3+溶液中的少量Al3+ | |
| C. | 将Fe(OH)3放入表面皿中,加入足量盐酸,将反应后的溶液加热蒸干、灼烧得到Fe2O3 | |
| D. | Al(OH)3中混有Mg(OH)2加入足量烧碱溶液,充分反应过滤,向滤液中加入足量盐酸后过滤、洗涤、干燥 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶粒可以导电 | B. | 胶体有丁达尔效应 | ||
| C. | 胶体粒子大小在1~100nm之间 | D. | 胶体的分散剂为气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 容器编号 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/min | |
| H2 | CO2 | HCOOH | |||
| Ⅰ | 150 | 0.4 | 0.4 | 0.2 | 2 |
| Ⅱ | 150 | 0.8 | 0.8 | t1 | |
| Ⅲ | 0.4 | 0.4 | 0.16 | t2 | |
| A. | 反应达到平衡时,容器Ⅰ中的平均反应速率为v(H2)=0.1mol/(L•min) | |
| B. | 反应达到平衡时,容器Ⅱ所需时间t2<2min | |
| C. | 若只改变一个反应条件,容器Ⅲ可能是加入了合适的催化剂 | |
| D. | 起始时,向容器Ⅱ中充入0.45mol H2、0.20mol CO2和0.18molHCOOH,则反应向正反应方向进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
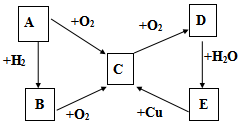 已知A、B、C、D、E五种物质有如图所示的转化关系(部分反应物及反应条件未列出,若解题时需要,可作合理假设),且五种物质中均含有A元素.
已知A、B、C、D、E五种物质有如图所示的转化关系(部分反应物及反应条件未列出,若解题时需要,可作合理假设),且五种物质中均含有A元素.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
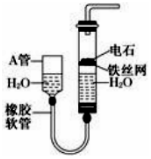 如图,图中的实验装置可用于制取乙炔.
如图,图中的实验装置可用于制取乙炔.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
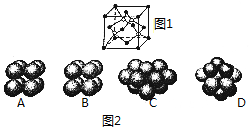 (1)碳化硅的晶胞结构(如图1)与金刚石类似(其中“●”为碳原子,“○”为硅原子).图2中“●”点构成的堆积方式与下列图示中D所表示的堆积方式相同
(1)碳化硅的晶胞结构(如图1)与金刚石类似(其中“●”为碳原子,“○”为硅原子).图2中“●”点构成的堆积方式与下列图示中D所表示的堆积方式相同查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | W与X形成的简单二元化合物的电子式为 | |
| B. | 短周期元素中Y的原子半径最大 | |
| C. | 工业上通过电解Y的氧化物制取Y的单质 | |
| D. | 最外层电子数等于其电子层数的金属与Z形成离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BaCl2溶液中通入足量的SO2气体后,所得溶液中2c(Ba2+)═c(Cl-) | |
| B. | 某溶液由水电离的c(H+)=1×10-amol/L,若a>7,则该溶液的pH一定为14-a | |
| C. | 物质的量浓度相等的H2S和NaHS混合溶液:c(Na+)═2c(S2-)+2c(HS-)+2c(H2S) | |
| D. | 常温下,若0.1mol/L NaHY溶液的pH=4,则该溶液中粒子浓度关系为:c(Na+)>c(HY-)>c(H2Y)>c(Y2-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com