
【题目】按照物质的树状分类法和交叉分类法,HNO3属于( )
①酸 ②氧化物 ③含氧酸 ④难挥发性酸 ⑤一元酸 ⑥化合物 ⑦混合物
A. ①②③④⑤⑥ B. ①③⑤⑥
C. ①②③⑤⑥⑦ D. ①③④⑤⑥
科目:高中化学 来源: 题型:
【题目】可逆反应mA(s)+n D(g)pX(g)+qY(g)在反应过程中,其他条件不变,D的转化率和温度T 或压强P关系如图所示(D%为D的转化率),下列叙述中正确的是( ) 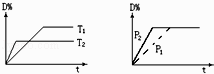
A.正反应为放热反应
B.使用催化剂,D的物质的量减小
C.化学方程式系数m+n=p+q
D.增加物质A或D的用量,平衡均向右移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知图一表示的是可逆反应CO(g)+H2(g)C(s)+H2O(g)△H>0的化学反应速率(v)与时间(t)的关系,图二表示的是可逆反应N2O4(g)2NO2(g)△H>0的浓度(c)随时间(t)的变化情况.下列说法中正确的是( ) 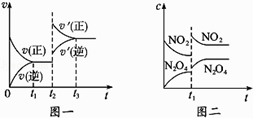
A.图一t2时改变的条件可能是升高了温度或增大了压强
B.图一t2时改变的条件是增大压强,则反应的△H增大
C.图二t1时改变的条件可能是升高了温度
D.若图二t1时改变的条件是增大压强,则混合气体的平均相对分子质量将增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】归纳法是高中化学学习常用的方法之一,某化学研究性学习小组在学习了《化学反应原理》后作出了如下的归纳总结:归纳正确的是( ) ①常温下,pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,则有c(Na+)+c(H+)=c(OH﹣)+c(CH3COO﹣)
②对已建立化学平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动时,生成物的百分含量一定增加
③常温下,AgCl在同物质的量浓度的CaCl2和NaCl溶液中的溶解度相同
④常温下,已知醋酸电离平衡常数为Ka;醋酸根水解平衡常数为Kh;水的离子积为Kw;KaKh=Kw
⑤电解精炼铜时,电解质溶液中铜离子浓度不变.
A.①④
B.①②④
C.①②④⑤
D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验。
I.将NaOH 溶液与NH4Cl 溶液混合生成NH3·H2O,从而验证NaOH 的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理? 并说明理由:______________________________。
II.根据下图所示装置图回答以下问题。
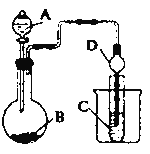
(1)利用如图装置可以验证非金属性的变化规律。干燥管D的作用是___________。
(2)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫:烧瓶中发生反应的离子方程式为_________。装置C中的实验现象为_________。
(3)若要用此装置证明非金属性: N>C>Si,从以下所给物质中选出甲同学设计的实验所用到物质:
①稀HNO3溶液 ②稀醋酸溶液 ③碳酸钙 ④Na2SiO3 溶液 ⑤SiO2
试剂A与C分别为______(填序号)。有同学认为此实验不能说明N、C、Si的非金属性强弱,你认为原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的非金属性在同周期元素中最强。下列说法不正确的是( )
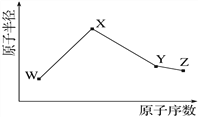
A. 对应简单离子半径:X>W
B. 对应简单气态氢化物的稳定性:Y<Z
C. Y的氧化物能与X的最高价氧化物对应的水化物反应
D. 化合物X2W2既含离子键也含共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(15分)凯氏定氨法是测定蛋白质中氮含量的经典方法,其原理是用浓硫酸在催化剂存在下将样品中有机氮转化成铵盐,利用如图所示装置处理铵盐,然后通过滴定测量.已知:NH3+H3BO3=NH3H3BO3;NH3H3BO3+HCl=NH4Cl+H3BO3 . 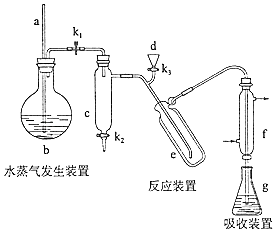
回答下列问题:
(1)a的作用是 .
(2)b中放入少量碎瓷片的目的是 . f的名称是 .
(3)清洗仪器:g中加蒸馏水:打开K1 , 关闭K2、K3 , 加热b,蒸气充满管路:停止加热,关闭K1 , g中蒸馏水倒吸进入c,原因是;打开K2放掉水,重复操作2~3次.
(4)仪器清洗后,g中加入硼酸(H3BO3)和指示剂,铵盐试样由d注入e,随后注入氢氧化钠溶液,用蒸馏水冲洗d,关闭K1 , d中保留少量水,打开K1 , 加热b,使水蒸气进入e.
①d中保留少量水的目的是 .
②e中主要反应的离子方程式为 , e采用中空双层玻璃瓶的作用是 .
(5)取某甘氨酸(C2H3NO2)样品m 克进行测定,滴定g中吸收液时消耗浓度为cmolL﹣1的盐酸V mL,则样品中氮的质量分数为%,样品的纯度≤%.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com