
下列关于葡萄糖的说法中,错误的是( )
A.葡萄糖的分子式是C6H12O6
B.葡萄糖是多羟基醛,因而具有醛和多元醇的性质
C.葡萄糖是最简单的醛糖
D.葡萄糖可以通过绿色植物光合作用合成
科目:高中化学 来源:2016-2017学年浙江省杭州市高一10月月考化学卷(解析版) 题型:选择题
某非金属单质A和氧气发生化合反应生成B,B为气体,其体积是反应掉氧气体积的两倍(同温同压)。关于B分子组成的推测一定正确的是( )
A.有1个氧原子 B.有2个氧原子
C.有1个A原子 D.有2个A原子
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二10月月考化学卷(解析版) 题型:选择题
已知热化学方程式:SO2(g)+1/2O2(g) SO3(g)△H=―98.32kJ/mol,下列表述正确的是( )
SO3(g)△H=―98.32kJ/mol,下列表述正确的是( )
A、在容器中充入2molSO2和1molO2充分反应,最终放出的热量等于196.6 4kJ
4kJ
B、在容器中当有2molSO2和1molO2发生反应时,放出的热量等于196.64kJ
C、在容器中当有4molSO2和2molO2发生反应时,反应SO2(g)+1/2O2(g) SO3(g)的反应热为-393.28kJ/mol
SO3(g)的反应热为-393.28kJ/mol
D、在容器中当有4molSO2和2molO2发生反应时,反应SO2(g)+1/2O2(g) SO3(g)的反应热为98.32kJ/mol
SO3(g)的反应热为98.32kJ/mol
查看答案和解析>>
科目:高中化学 来源:2016-2017学年内蒙古高二上期中化学卷(解析版) 题型:选择题
L-多巴是一种有机物,它可用于帕金森综合症的治疗,其结构简式为:
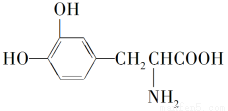
这种药物的研制是基于获得2000年诺贝尔生理学或医学奖和获得2001年诺贝尔化学奖的研究成果。下列关于L-多巴酸碱性的叙述正确的是( )
A.既没有酸性,又没有碱性 B.既具有酸性,又具有碱性
C.只有酸性,没有碱性 D.只有碱性,没有酸性
查看答案和解析>>
科目:高中化学 来源:2016-2017学年内蒙古高二上期中化学卷(解析版) 题型:选择题
某有机物与过量的金属钠反应,得到VA L气体,另一份等质量的该有机物与纯碱反应得到气体VB L(同温、同压),若VA>VB,则该有机物可能是( )
A. HOCH2CH2OH B.CH3COOH
C. HOOC—COOH D.HOOC—C6H4—OH
HOOC—COOH D.HOOC—C6H4—OH
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高二上期中化学卷(解析版) 题型:填空题
(1)反应Fe(s)+CO2(g) FeO(s)+CO(g) ΔH1,平衡常数为K1;
FeO(s)+CO(g) ΔH1,平衡常数为K1;
反应Fe(s)+H2O(g) FeO(s)+H2(g) ΔH2,平衡常数为K2。
FeO(s)+H2(g) ΔH2,平衡常数为K2。
在不同温度时K1、K2的值如下表:
700℃ | 900℃ | |
K1 | 1.47 | 2.15 |
K2 | 2.38 | 1.67 |
①反应 CO2(g) + H2(g) CO(g) + H2O(g) ΔH,平衡常数K,则ΔH = (用ΔH1和ΔH2表示),K= (用K1和K2表示),且由上述计算可知,反应CO2(g) + H2(g)
CO(g) + H2O(g) ΔH,平衡常数K,则ΔH = (用ΔH1和ΔH2表示),K= (用K1和K2表示),且由上述计算可知,反应CO2(g) + H2(g) CO(g) + H2O(g)是 反应(填“吸热”或“放热”)。
CO(g) + H2O(g)是 反应(填“吸热”或“放热”)。
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+CO2(g) FeO(s)+CO(g) ΔH > 0,CO2的浓度与时间的关系如图所示:
FeO(s)+CO(g) ΔH > 0,CO2的浓度与时间的关系如图所示:
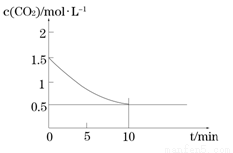
① 该条件下反应的平衡常数为 ;
② 下列措施中能使平衡时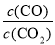 增大的是 (填序号)
增大的是 (填序号)
A.升高温度 B.增大压强
C.充入一定量的CO2 D.再加入一定量铁粉
③ 一定温度下,在一个固定容积的密闭容器中发生上述反应,下列能判断该反应达到化学平衡状态的是 (填字母)。
a.容器中压强不变
b.气体的密度不再改变
c.v正(CO2)=v逆(CO)
d.c(CO2)=c(CO)
e.容器内气体总物质的量不变
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高二上期中化学卷(解析版) 题型:选择题
为了证明醋酸是弱电解质,四同学分别进行实验:甲用pH试纸测出0.10 mol/L的醋酸溶液pH = 4;乙将pH = 3醋酸和盐酸,各取10 mL,用蒸馏水稀释到原来的100倍,然后用pH试纸测定该溶液的pH,醋酸的变化小;丙将pH = 3醋酸和盐酸,分别加入相应的钠盐固体,醋酸的pH变化大;丁取pH = 3醋酸和盐酸,分别稀释到原来的100倍,然后加入完全一样的锌粒,测量醋酸放出H2的速率快。
A.一位同学 B.二位同学 C.三位同学 D.四位同学
查看答案和解析>>
科目:高中化学 来源:2017届湖北省襄阳市四校高三上学期期中化学试卷(解析版) 题型:填空题
A、B、C、D、E、W为六种前四周期元素,它们的原子序数依次增大。A与D同主族,可形成DA型离子化合物,B与C同周期且相邻,C与E同主族,E2-与Ar原子具有相同的电子层结构,W的合金用量最大、用途最广。请回答下列问题:
(1)W元素在元素周期表中的位置为 。
(2)下列说法正确的是( )
A.原子半径:A<B<C<D<E
B.D2WC4可以用来做消毒剂和净水剂
C.A4B2C3中既含有离子键又含有共价键
D.D2C2与EC2可以反应生成D2EC3和C2
(3)灼热的碳能与B的最高价氧化物对应水化物的浓溶液反应,化学反应方程式为 。
(4)向盛有A2C2溶液的试管中加入几滴酸化的WEC4溶液,溶液变成棕黄色,发生反应的离子方程式为 ;一段时间后,溶液中有大量气泡出现,随后溶液温度升高,有红褐色沉淀生成,则产生气泡的原因是 ;生成沉淀的原因是 (用平衡移动原理解释)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高一上期中考试化学试卷(解析版) 题型:计算题
将50g密度ρ=0.98g/mL的10%的氨水和100g密度ρ=0.93g/mL的40%的氨水混合,得到ρ=0.95g/mL氨水溶液,求所得氨水的物质的量浓度是多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com