
短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13。X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍也是Y原子最外层电子数的3倍。下列说法正确的是( )
A.Y与Z形成的简单离子核外电子排布相同
B.X的氧化物为离子化合物
C.Z的氢化物的水溶液在空气中容易变质
D.X与Z对应的氧化物的水化物一定为强酸
科目:高中化学 来源:2014高考化学名师选择题专练 离子反应练习卷(解析版) 题型:选择题
下列离子方程式书写正确的是( )
A.Na2O2与H2O反应:2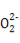 +2H2O
+2H2O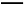 4OH-+O2↑
4OH-+O2↑
B.FeCl2溶液与稀硝酸反应:Fe2++N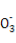 +4H+
+4H+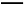 Fe3++NO↑+2H2O
Fe3++NO↑+2H2O
C.CaCO3与醋酸溶液反应:CaCO3+2H+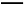 Ca2++CO2↑+H2O
Ca2++CO2↑+H2O
D.KAl(SO4)2溶液与氨水反应:Al3++3NH3·H2O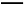 Al(OH)3↓+3N
Al(OH)3↓+3N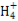
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 化学反应中的能量变化练习卷(解析版) 题型:选择题
上海世博会中国馆、主题馆等建筑使用光伏并网发电,总功率达4兆瓦,是历届世博会之最。已知发出白光的LED是由氮化镓GaN芯片与钇铝石榴石(YAG,化学式:Y3Al5O12)芯片封装在一起做成的。下列有关叙述正确的是( )
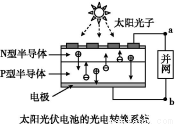
A.光伏电池实现了太阳能和电能的相互转化
B.图中N型半导体为正极,P型半导体为负极
C.电流从a流向b
D.LED中的Ga和Y都显+3价
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 化学与STSE练习卷(解析版) 题型:选择题
党的十八大报告提出了“建设美丽中国”的宏伟蓝图。节能减排、低碳生活、合理利用资源、保护环境,走可持续发展的道路成为我国发展的重要战略。下列说法不符合这一主题思想的是( )
A.大力开采我省陇东地区的煤和石油,促进地方经济发展
B.实施矿物燃料“脱硫、脱硝技术”,减少硫的氧化物和氮的氧化物污染
C.积极推广太阳能、风能、地热能等新能源的使用,减少化石燃料的使用,有效降低PM2.5对环境的污染
D.对城市生活污水脱氮除磷、净化处理,遏制水体富营养化
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 元素周期表元素周期律练习卷(解析版) 题型:选择题
现有X、Y、Z、W、Q五种短周期元素,原子序数依次增大,Y、Z、W、Q形成的简单离子具有相同的电子层结构,YX3、X2Z、X2Z2、W2Z、W2Z2都是常见的化合物,其中,YX3在常温下呈气态,能使酚酞溶液变红色。下列有关推断正确的是( )
A.简单离子半径:Y>Z>W>Q>X
B.W2Z2与X2Z反应中氧化剂与还原剂物质的量之比为1∶2
C.X能分别与Y、Z、W形成共价化合物
D.Y、W、Q的最高价氧化物对应的水化物两两之间一定相互反应
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 NA的应用练习卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A.1 mol羟基与17 g NH3所含电子数都为NA
B.12.4 g白磷(分子式为P4)中含有P—P共价键0.6NA
C.电解精炼铜的过程中,每转移NA个电子时,阳极溶解铜的质量为32 g
D.适量铜粉溶解于1 L 0.5 mol/L稀硝酸中,当生成2.24 L NO时,溶液中氮原子数为0.4NA
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 NA的应用练习卷(解析版) 题型:选择题
设NA代表阿伏加德罗常数的值,下列说法中正确的是( )
A.1 mol NaHSO4晶体含有2NA个离子
B.1 L 2 mol/L明矾溶液经水解可得到氢氧化铝胶体粒子的数目为2NA
C.1 mol C (碳正离子)中含有的电子数为10NA
(碳正离子)中含有的电子数为10NA
D.在O2参与的反应中,1 mol O2作氧化剂时得到的电子数一定是4NA
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师综合题专练 物质性质综合应用练习卷(解析版) 题型:填空题
某研究小组将一批废弃的线路板经浓硝酸和稀硫酸处理后得到一混合溶液,其中含有Cu2+、Fe2+、Fe3+、Al3+等金属离子,并设计了以下两种流程以分别制取CuSO4·5H2O晶体和AlCl3
溶液:
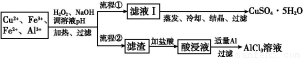
已知:相关金属离子开始沉淀至完全沉淀时的pH范围为:
离子 | Fe3+ | Fe2+ | Al3+ | Cu2+ |
pH范围 | 2.2~3.2 | 5.5~9.0 | 4.1~5.0 | 5.3~6.6 |
请回答下列问题:
(1)加入H2O2的作用是 ,欲使制取的CuSO4·5H2O晶体较为纯净,pH至少应调至 。
(2)写出H2O2与Fe2+反应的离子方程式: 。
(3)流程②中加入适量Al粉起的作用是 。
(4)根据你所学的化学知识,由AlCl3溶液(不添加其他化学试剂)能否制得无水AlCl3 (填“能”或“不能”),原因是 。
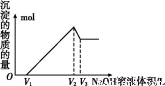
(5)取体积为V(L)的酸浸液,向其中滴加a mol·L-1的NaOH溶液,生成沉淀的物质的量与所加的NaOH溶液的体积(L)关系如图。请用V1、V2、V3表示所取的酸浸液中n(Fe3+)∶n(Al3+)= 。
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 选修2化学与技术练习卷(解析版) 题型:选择题
下列使用化肥、农药的描述中正确的是( )
A.高温多雨时比较适合施用钾肥
B.长期施用硫铵会造成土壤板结
C.石硫合剂必须与硫酸混合后才能施用
D.草木灰可以和铵态氮肥一块施用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com