
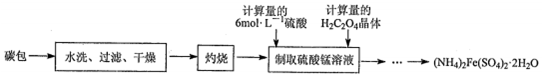
·ÖĪö ·Ļ¾Éøɵē³ŲĢ¼°ü”¾ŗ¬MnO2ŗĶÉŁĮæµÄMnO£ØOH£©”¢C”¢NH4Cl”¢ZnCl2”¢µķ·Ūŗż¼°FeµČ”棬NH4Cl”¢ZnCl2ČÜÓŚĖ®£¬Ė®Ļ“æɳżČ„£¬¹żĀĖ”¢øÉŌļµĆµ½MnO2ŗĶÉŁĮæµÄMnO£ØOH£©”¢C”¢µķ·Ūŗż¼°FeµÄ»ģŗĻĪļ£¬×ĘÉÕøĆ»ģŗĻĪļ£¬³żČ„C¼°µķ·ŪŗżµČ£¬µĆµ½¹ĢĢåMnO2ŗĶÉŁĮæµÄMnO£ØOH£©”¢Fe2O3£¬¾ĄäČ“ŗóŠčŅŖ½ųŠŠ³ĘĮ棬¼ÓČė¼ĘĖćĮæµÄĮņĖįŗĶH2C2O4•2H2O¾§Ģå£ŗMnO2+H2C2O4+H2SO4$\frac{\underline{\;Ī¢ČČ\;}}{\;}$Mn£ØSO4£©2+2CO2”ü+2H2O£¬µĆµ½ĮņĖįĆĢČÜŅŗŗ¬ÉŁĮæFe2£ØSO4£©3ŌÓÖŹ£¬ĻņČÜŅŗÖŠ±ß½Į°č±ßĻņČÜŅŗÖŠ¼ÓČėMn£ØOH£©2£¬ÖĮ4.1£¼pH£¼7.8£¬¹żĀĖ£¬±ß½Į°č±ßĻņĀĖŅŗÖŠ¼ÓČė¼ĘĖćĮæµÄ£ØNH4£©2SO4¹ĢĢ壬Ī¢ČČŹ¹ĘäČܽā£¬Õō·¢ÅØĖõÖĮ±ķĆę³öĻÖ¾§Ä¤£¬ĄäČ“ÖĮŹŅĪĀ£¬¹żĀĖ£¬ÓĆŅŅ“¼Ļ“µÓ2”«3“Ī¾§Ģ壬ĀĖÖ½ĪüøÉ£¬µĆµ½£ØNH4£©2Mn£ØSO4£©2•2H2O£¬¾Ż“Ė·ÖĪö½ā“š£®
½ā“š ½ā£ŗ£Ø1£©×ĘÉÕŠčŅŖÓƵ½µÄ¹čĖįŃĪÖŹŅĒĘ÷ÓŠ²£Į§°ō”¢ÄąČż½Ē”¢ŪįŪöŗĶ¾Ę¾«µĘ£»C”¢µķ·ŪŗżŹÜČČ·Ö½āÉś³É¶žŃõ»ÆĢ¼ŗĶĖ®£¬æÉÓė¶žŃõ»ÆĆĢµČ·ÖĄė£¬¹Ź×ĘÉÕæɳżČ„C¼°µķ·ŪŗżµČ£»
¹Ź“š°øĪŖ£ŗĹȿ½Ē”¢ŪįŪöŗĶ¾Ę¾«µĘ£»³żČ„C¼°µķ·ŪŗżµČ£»
£Ø2£©ÓÉĮ÷³ĢæÉÖŖ£¬ĮņĖį”¢²ŻĖį¼°ĮņĖįļ§µÄ¼ÓČėŠčŅŖČ·¶ØĮ棬¹Ź”°×ĘÉÕ”±ŗóµÄ¹ĢĢå¾ĄäČ“ŗóŠčŅŖ½ųŠŠ³ĘĮ棬±ćÓŚ¼ĘĖćČ·¶ØŠč¼ÓČėµÄĮņĖį”¢²ŻĖį¼°ĮņĖįļ§µÄĮ棻
¹Ź“š°øĪŖ£ŗ±ćÓŚ¼ĘĖćČ·¶ØŠč¼ÓČėµÄĮņĖį”¢²ŻĖį¼°ĮņĖįļ§µÄĮ棻
£Ø3£©MnO2±»»¹ŌĪŖMnSO4µÄ»Æѧ·½³ĢŹ½ĪŖMnO2+H2C2O4+H2SO4$\frac{\underline{\;Ī¢ČČ\;}}{\;}$Mn£ØSO4£©2+2CO2”ü+2H2O£¬ĘäÖŠĀżĀż·Ö“Ī¼ÓČėH2C2O4•2H2O£¬æÉŅŌæŲÖĘ·“Ó¦ĖŁĀŹ£¬·ĄÖ¹Ģ¼°üÅŻÄ³å³öČŻĘ÷£»
¹Ź“š°øĪŖ£ŗæŲÖĘ·“Ó¦ĖŁĀŹ£¬·ĄÖ¹Ģ¼°üÅŻÄ³å³öČŻĘ÷£»MnO2+H2C2O4+H2SO4$\frac{\underline{\;Ī¢ČČ\;}}{\;}$Mn£ØSO4£©2+2CO2”ü+2H2O£»
£Ø4£©ĮņĖįĆĢČÜŅŗ[ŗ¬ÉŁĮæFe2£ØSO4£©3ŌÓÖŹ£¬¼ÓČėMn£ØOH£©2µ÷½ŚpH“Ł½ųĢśĄė×ÓµÄĖ®½ā±ćÓŚÉś³É³Įµķ³żČ„£¬ŅŃÖŖČÜŅŗÖŠpH=7.8Ź±Mn£ØOH£©2æŖŹ¼³Įµķ£»pH=4.1Ź±Fe£ØOH£©3³ĮµķĶźČ«£¬¹ŹpH·¶Ī§ĪŖ4.1£¼pH£¼7.8£¬¹żĀĖŗ󣬼ÓČė£ØNH4£©2SO4¹ĢĢ壬Õō·¢ÅØĖõµĆµ½£ØNH4£©2Mn£ØSO4£©2•2H2O£¬¾ßĢå²Ł×÷ĪŖ£ŗĻņČÜŅŗÖŠ±ß½Į°č±ßĻņČÜŅŗÖŠ¼ÓČėMn£ØOH£©2£¬ÖĮ4.1£¼pH£¼7.8£¬¹żĀĖ£¬±ß½Į°č±ßĻņĀĖŅŗÖŠ¼ÓČė¼ĘĖćĮæµÄ£ØNH4£©2SO4¹ĢĢ壬Ī¢ČČŹ¹ĘäČܽā£¬Õō·¢ÅØĖõÖĮ±ķĆę³öĻÖ¾§Ä¤£¬ĄäČ“ÖĮŹŅĪĀ£¬¹żĀĖ£¬ÓĆŅŅ“¼Ļ“µÓ2”«3“Ī¾§Ģ壬ĀĖÖ½ĪüøÉ£¬µĆµ½£ØNH4£©2Mn£ØSO4£©2•2H2O£»
¹Ź“š°øĪŖ£ŗÖĮ4.1£¼pH£¼7.8£¬¹żĀĖ£¬±ß½Į°č±ßĻņĀĖŅŗÖŠ¼ÓČė¼ĘĖćĮæµÄ£ØNH4£©2SO4¹ĢĢ壬Ī¢ČČŹ¹ĘäČܽā£¬Õō·¢ÅØĖõÖĮ±ķĆę³öĻÖ¾§Ä¤£¬ĄäČ“ÖĮŹŅĪĀ£¬¹żĀĖ£¬ÓĆŅŅ“¼Ļ“µÓ2”«3“Ī¾§Ģ壮
µćĘĄ ±¾Ģāæ¼²éĮĖĪļÖŹµÄÖʱø£¬Éę¼°¶Ō¹¤ŅÕĮ÷³ĢµÄĄķ½ā”¢Ńõ»Æ»¹Ō·“Ó¦”¢¶ŌĢõ¼žµÄæŲÖĘŃ”ŌńÓėĄķ½āµČ£¬Ąķ½ā¹¤ŅÕĮ÷³ĢŌĄķŹĒ½āĢāµÄ¹Ų¼ü£¬ŹĒ¶Ōѧɜ×ŪŗĻÄÜĮ¦µÄ漲飬ŠčŅŖѧɜ¾ß±øŌśŹµµÄ»ł“”ÓėĮé»īŌĖÓĆÄÜĮ¦£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
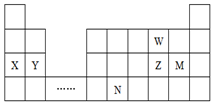
| A£® | Ō×Ó°ė¾¶£ŗY£¾Z£¾W£¬¼ņµ„Ąė×Ó°ė¾¶£ŗM-£¾Z2-£¾W2- | |
| B£® | µ„ÖŹµÄ»¹ŌŠŌ£ŗX£¾Y£¬¼ņµ„Ēā»ÆĪļµÄ·Šµć£ŗZ£¾W | |
| C£® | äåÓėŌŖĖŲMĶ¬Ö÷×壬×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļµÄĖįŠŌ±ČMµÄĒæ | |
| D£® | ŌŖĖŲNĪ»ÓŚ½šŹōÓė·Ē½šŹōµÄ·Ö½ēĻßø½½ü£¬æÉŅŌĶʶĻNµÄµ„ÖŹæÉ×÷ °ėµ¼Ģå²ÄĮĻ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ”÷H2£¾0 | |
| B£® | BĪŖH2ŗĶO2ÖʱøH2O2µÄ“߻ƼĮ | |
| C£® | ·“Ó¦¢ŁµÄÕż·“Ó¦µÄ»ī»ÆÄÜ“óÓŚÄę·“Ó¦µÄ»ī»ÆÄÜ | |
| D£® | H2£Øg£©+O2£Øg£©?H2O2£Ø1£©µÄ”÷H£¼0 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ź±¼ä/s | 0 | 1 | 2 | 3 | 4 |
| C£ØNO£©/mol•L-1 | 9.50”Į10-3 | 4.50”Į10-3 | 2.50”Į10-5 | 1.50”Į10-3 | 1.5”Į10-3 |
| C£ØCO£©/mol•L-1 | 9.00”Į10-3 | 4.00”Į10-3 | 2.00”Į10-3 | 1.00”Į10-3 | 1.00”Į10-3 |
| A£® | -¶ØĪĀ¶ČĻĀ£¬“ÓæŖŹ¼µ½Ę½ŗā£¬øĆ·“Ó¦µÄĘ½ŗā³£ŹżÖš½„Ōö“ó | |
| B£® | Ē°2sÄŚµÄĘ½¾ł·“Ó¦ĖŁĀŹv£ØN2£©=1.75”Į10-3 mol•L-1•s-1 | |
| C£® | “ļµ½Ę½ŗāŹ±£¬COµÄ×Ŗ»ÆĀŹĪŖ11.11% | |
| D£® | 3sŹ±NOŗĶCOµÄÅØ¶Č¶¼²»ŌŁ±ä»Æ£¬·“Ó¦Ķ£Ö¹½ųŠŠ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | Ņż·¢øĆ·“Ó¦Ņ»¶ØŠčŅŖ¼ÓČČ»ņµćČ¼µČĢõ¼ž | |
| B£® | E1Äę·“Ó¦µÄ»ī»ÆÄÜ£¬E2ŹĒÕż·“Ó¦µÄ»ī»ÆÄÜ | |
| C£® | “߻ƼĮÄܼõŠ”E1ŗĶE2£¬µ«²»øı䷓ӦµÄģŹ±ä | |
| D£® | X”¢Y”¢Z±ķŹ¾µÄ·“Ó¦ĖŁĀŹÖ®±ČĪŖ2£ŗ1£ŗ1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NH3Ņ×Ņŗ»Æ£¬°±³£ÓĆ×÷ÖĘĄä¼Į | |
| B£® | µØ·ÆÓöÅØĮņĖį±ä°×ŹĒŅņĪŖÅØĮņĖįµÄĶŃĖ®ŠŌ | |
| C£® | °±“ß»ÆŃõ»ÆÖĘĻõĖį¹ż³ĢÖŠµÄČżøöÖ÷ŅŖ·“Ó¦¶¼ŹōÓŚŃõ»Æ»¹Ō·“Ó¦ | |
| D£® | ÅØĻõĖįŠč±£“ęŌŚ×ŲÉ«ĘæÖŠ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2ÖÖ | B£® | 3ÖÖ | C£® | 4ÖÖ | D£® | 5ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1 molŅŅĻ©ŗĶŅŅ“¼µÄ»ģŗĻĪļĶźČ«Č¼ÉÕŹ±ĻūŗÄO2µÄ·Ö×ÓŹżĪŖ3NA | |
| B£® | 1.5 mol Na2OŗĶNa2O2µÄ»ģŗĻĪļÖŠĄė×ÓŹżÄæĪŖ4.5 NA | |
| C£® | ±ź×¼×“æöĻĀ£¬11.2 L HFÖŠŗ¬ÓŠµÄ·Ö×ÓŹżĪŖ0.5NA | |
| D£® | ³£ĪĀ³£Ń¹ĻĀ£¬17 g ōĒ»łŗ¬ÓŠµÄµē×Ó×ÜŹżĪŖ9 NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na2O2ŗĶKMnO4·Ö±šÖʵĆ1molO2×ŖŅʵĵē×ÓŹż¾łŹĒ4NA | |
| B£® | ±ź×¼×“æöĻĀ£¬11.2LŅŅĻ©ŗĶ»·±ūĶé£ØC3H6£©µÄ»ģŗĻĘųĢåÖŠ£¬¹²ÓƵē×Ó¶ŌµÄŹżÄæĪŖ3NA | |
| C£® | Čō1L 0.2mol/LµÄFeCl3ČÜŅŗĶźČ«Ė®½āŠĪ³É½ŗĢ壬Ōņ½ŗĢåĪ¢Į£ŹżĪŖ0.2NA | |
| D£® | ÓƶčŠŌµē¼«µē½ā1L0£®lmol•L-1µÄŹ³ŃĪĖ®£¬Į½¼«¹²ŹÕ¼Æµ½0.28molµÄĘųĢ壬ŌņµēĀ·ÖŠ×ŖŅʵē×ÓŹżĪŖ0.34NA£Ø²»æ¼ĀĒĘųĢåµÄČܽā£© |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com