
| 选项 | 物质 | 所用试剂 | 方法 |
| A | 乙醇(乙酸) | 氢氧化钠溶液 | 分液 |
| B | 乙烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| C | 乙酸乙酯(乙酸) | 饱和碳酸钠溶液 | 蒸馏 |
| D | 乙醇(水) | 生石灰 | 蒸馏 |
| A.A | B.B | C.C | D.D |
 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.除去甲烷中混有的少量乙烯:氢气 |
| B.除去乙酸乙酯中混有的少量乙酸:乙醇 |
| C.除去溴苯中混有的少量溴单质:氢氧化钠溶液 |
| D.除去苯中混有的少量苯酚:浓溴水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
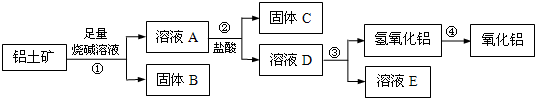
| A.沉淀X的成分是SiO2 |
| B.溶液Y中的阳离子主要是Mg2+、Al3+、Fe3+、H+ |
| C.将试样直接溶于过量的NaOH溶液后过滤,可得到红色颜料Fe2O3 |
| D.在Y中加入过量的NaOH溶液,过滤得到的沉淀的主要成分是Fe(OH)3和Mg(OH)2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:多选题
| A.用酒精萃取碘水中的碘 |
| B.用蒸馏的方法将自来水制成蒸馏水 |
| C.用蒸发食盐水的方法得到氯化钠晶体 |
| D.用过滤的方法分离二氧化硅和氧化钙的混合物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 物质 | 试剂 | 方法 |
| (1)乙烷(乙烯) | ______ | ______ |
| (2)溴苯(溴) | ______ | ______ |
| (3)乙醇(水) | ______ | ______ |
| (4)乙酸乙酯(乙酸) | ______ | ______ |
| (5)苯甲酸(NaCl) | ______ | ______ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
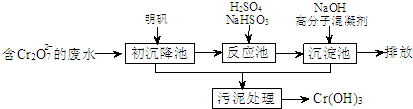
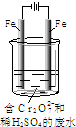
| 开始沉淀的pH | 完全沉淀的pH | |
| Fe(OH)2 | 7.0 | 9.0 |
| Fe(OH)3 | 1.9 | 3.2 |
| Cr(OH)3 | 6.0 | 8.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com