
 某种食品的配料标签如图所示.
某种食品的配料标签如图所示.分析 ①瘦肉类、蛋类、豆类富含蛋白质,植物油和动物脂肪富含油脂;
②蛋白质水解生成氨基酸,蛋白质能发生盐析;
③苯甲酸钠是防腐剂,碳酸氢钠受热分解生成碳酸钠、水和二氧化碳;
④淀粉遇碘变蓝色.
解答 解:①瘦肉类、蛋类、豆类富含蛋白质,因此鸡蛋富含蛋白质,植物油和动物脂肪富含油脂,因此棕榈油富含油脂,
故答案为:鸡蛋;棕榈油;
②蛋白质在一定条件下水解生成氨基酸,在蛋白质溶液中加入饱和硫酸铵溶液能发生盐析,即有白色沉淀析出;
故答案为:氨基酸;盐析;
③苯甲酸钠是防腐剂有防腐作用,碳酸氢钠受热分解生成碳酸钠、水和二氧化碳,方程式为2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,
故答案为:苯甲酸钠;2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;
④淀粉遇碘变蓝色,可以利用碘的这种性质检验淀粉的存在,故答案为:滴加碘水溶液变蓝色.
点评 本题考查知识点较多,注重化学与生活的联系,熟悉常见的环境污染物,并关注环境保护,利用化学知识来解决生活中的问题即可解答,题目难度不大.


科目:高中化学 来源: 题型:解答题
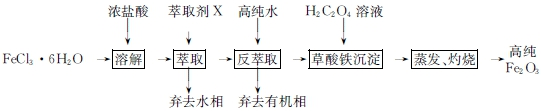
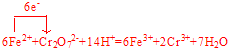 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.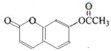 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业制备NaClO可用电解饱和食盐水的方法离子方程式为:Cl-+H2O $\frac{\underline{\;电解\;}}{\;}$ ClO-+H2↑ | |
| B. | 向NaClO溶液中通入少量SO2气体离子方程式为:SO2+3ClO-+2H2O═2HClO+SO42-+Cl- | |
| C. | 在NaClO溶液中可以大量共存的离子有:K+,SO42-,Fe3+,NO3- | |
| D. | 84消毒液不能和洁厕剂混合使用,也不能用pH试纸测其pH值. |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 12mL | B. | 15 mL | C. | 19mL | D. | 31mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 还原性强弱:F->Cl->I- | B. | 原子半径大小:Na>S>O | ||
| C. | 碱性强弱:KOH>NaOH>LiOH | D. | 稳定性强弱:HF>HCl>HBr |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com