
【题目】常温下将NaOH溶液添加到己二酸(H2X)溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述错误的是

A.Ka2(H2X)的数量级为10-6
B.曲线N表示pH与![]() 的变化关系
的变化关系
C.NaHX溶液中c(H+)>c(OH-)
D.当混合溶液呈中性时,c(Na+)>c(HX-)>c(X2-)>c(H+)=c(OH-)
【答案】D
【解析】A、Ka2=![]() ,己二酸是弱酸,第二步电离小于第一步,曲线M是己二酸的第二步电离,根据图像,取-0.6和4.8点,
,己二酸是弱酸,第二步电离小于第一步,曲线M是己二酸的第二步电离,根据图像,取-0.6和4.8点,![]() =10-0.6mol·L-1,c(H+)=10-4.8mol·L-1,代入Ka2,得到Ka2=10-5.4=10-6+0.6=100.6*10-6=3.98*10-6,A正确;B.当
=10-0.6mol·L-1,c(H+)=10-4.8mol·L-1,代入Ka2,得到Ka2=10-5.4=10-6+0.6=100.6*10-6=3.98*10-6,A正确;B.当![]() =0或lg
=0或lg![]() =0,溶液中c(H2X)=c(HX-),c(X2-)=c(HX-),溶液中c(H2X)=c(HX-)时溶液的酸性强,即pH小,则曲线N表示pH与
=0,溶液中c(H2X)=c(HX-),c(X2-)=c(HX-),溶液中c(H2X)=c(HX-)时溶液的酸性强,即pH小,则曲线N表示pH与![]() 的关系,B正确;C.在NaHX溶液中,此时lg
的关系,B正确;C.在NaHX溶液中,此时lg![]() <0,溶液显酸性,即c(H+)>c(OH-),C正确;D.当混合溶液呈中性时,c(H+)=c(OH-),lg
<0,溶液显酸性,即c(H+)>c(OH-),C正确;D.当混合溶液呈中性时,c(H+)=c(OH-),lg![]() >1,即c(X2-)>c(HX-),D错误;答案选D。
>1,即c(X2-)>c(HX-),D错误;答案选D。


科目:高中化学 来源: 题型:
【题目】写出下列反应的化学反应方程式:(要求写出反应条件)
(1)甲烷与氯气反应生成一氯甲烷 ______________________________________
(2)苯与浓硝酸发生取代反应:________________________________________________
(3)溴乙烷与 NaOH的乙醇溶液加热:_________________________________ (4)乙醇制乙烯:__________________________________
(5)将灼热的铜丝浸入乙醇中: _________________________________ (6)苯酚制三溴苯酚:_____________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无机化合物可根据其组成和性质进行分类:

(1)上图所示的物质分类方法名称是________。
(2)以Na、K、H、O、C、S、N中任两种或三种元素组成合适的物质,分别填在下表②③⑥ 的后面。
物质类别 | 酸 | 碱 | 盐 | 氧化物 |
化学式 | ①HCl ②____ | ③______ ④Ba(OH)2 | ⑤Na2CO3 ⑥______ | ⑦CO2 ⑧Na2O2 |
(3)写出⑦转化为⑤的化学方程式:______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2L恒容密闭容器中,X、Y、Z三种气态物质的变化曲线如图所示,关于其变化的一些说法正确的是
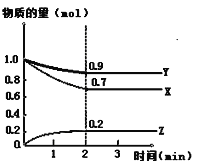
A. 用X表示该化学反应速率比用Y表示的要快
B. 该反应的化学方程式:3X+Y![]() 2Z
2Z
C. 若在3min后,把Z从反应体系中分离,平衡不移动
D. 反应开始至2min,Z的平均反应速率:0.1mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列反应中,HCl作还原剂的是( )
A. NaOH + HCl = NaCl + H2O
B. Zn + 2HCl = ZnCl2 + H2↑
C. MnO2 + 4HCl(浓)![]() MnCl2 + 2H2O + Cl2↑
MnCl2 + 2H2O + Cl2↑
D. CuO + 2HCl = CuCl2 + H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】支撑海港码头基础的钢管柱,常用外加电流的阴极保护法进行防腐,工作原理如图所示,其中高硅铸铁为惰性辅助阳极。下列有关表述不正确的是
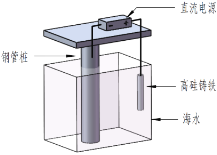
A.通入保护电流使钢管桩表面腐蚀电流接近于零
B.通电后外电路电子被强制从高硅铸铁流向钢管桩
C.高硅铸铁的作用是作为损耗阳极材料和传递电流
D.通入的保护电流应该根据环境条件变化进行调整
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上合成氨采用500℃左右的温度,其原因是:①适当加快NH3的合成速率 ②提高氢气的转化率 ③提高氨的产率 ④催化剂在500℃左右活性最好
A.①B.①③C.①④D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知和碳元素同主族的X元素位于元素周期表中的第一个长周期,短周期元素Y原子的最外层电子数比内层电子总数少3,它们形成化合物的分子式是XY4。试回答:
(1)X元素的原子基态时电子排布式为: ____________________________,
Y元素原子最外层电子的电子排布图为:____________________________。
(2)若X、Y两元素电负性分别为2.1和2.85,试判断XY4中X与Y之间的化学键为____(填“共价键”或“离子键”)。
(3)该化合物的空间结构为____,中心原子的杂化类型为____,分子为____(填“极性分子”或“非极性分子”)。
(4)该化合物在常温下为液体,该液体微粒间的作用力是____。
(5)该化合物的沸点与SiCl4比较:____(填化学式)的高,原因是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(14分)H2S和SO2会对环境和人体健康带来极大的危害,工业上采取多种方法减少这些有害气体的排放,回答下列方法中的问题。
Ⅰ.H2S的除去
方法1:生物脱H2S的原理为:
H2S+Fe2(SO4)3![]() S↓+2FeSO4+H2SO4
S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4![]() 2Fe2(SO4)3+2H2O
2Fe2(SO4)3+2H2O
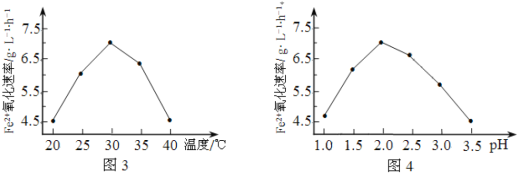
(1)硫杆菌存在时,FeSO4被氧化的速率是无菌时的5×105倍,该菌的作用是______________。
(2)由图3和图4判断使用硫杆菌的最佳条件为______________。若反应温度过高,反应速率下降,其原因是______________。
方法2:在一定条件下,用H2O2氧化H2S
(3)随着参加反应的n(H2O2)/n(H2S)变化,氧化产物不同。当n(H2O2)/n(H2S)=4时,氧化产物的分子式为__________。
Ⅱ.SO2的除去
方法1(双碱法):用NaOH吸收SO2,并用CaO使NaOH再生
NaOH溶液![]() Na2SO3
Na2SO3
(4)写出过程①的离子方程式:____________________________;CaO在水中存在如下转化:
CaO(s)+H2O (l) ![]() Ca(OH)2(s)
Ca(OH)2(s)![]() Ca2+(aq)+2OH(aq)
Ca2+(aq)+2OH(aq)
从平衡移动的角度,简述过程②NaOH再生的原理____________________________________。
方法2:用氨水除去SO2
(5)已知25℃,NH3·H2O的Kb=1.8×105,H2SO3的Ka1=1.3×102,Ka2=6.2×108。若氨水的浓度为2.0 mol·L-1,溶液中的c(OH)=_________________mol·L1。将SO2通入该氨水中,当c(OH)降至1.0×107 mol·L1时,溶液中的c(![]() )/c(
)/c(![]() )=___________________。
)=___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com