
| A. | 过量的SO2通入NaOH溶液中:SO2+2OH-═SO32-+H2O | |
| B. | 用醋酸溶解CaCO3:2H+CaCO3═Ca2++H2O+CO2↑ | |
| C. | 在氯化亚铁溶液中通入氯气Fe2++Cl2═Fe3++2Cl- | |
| D. | NaHCO3溶液中加入过量的Ba(OH)2溶液:HCO3-+Ba2++OH-═BaCO3↓+H2O |
分析 A.反应生成亚硫酸氢钠;
B.醋酸在离子反应中保留化学式;
C.电子、电荷不守恒;
D.碳酸氢钠完全反应,生成碳酸钡、NaOH和水.
解答 解:A.过量的SO2通入NaOH溶液中的离子反应为SO2+OH-═HSO3-,故A错误;
B.用醋酸溶解CaCO3的离子反应为CaCO3+2CH3COOH═2CH3COO-+Ca2++CO2↑+H2O,故B错误;
C.在氯化亚铁溶液中通入氯气的离子反应为2Fe2++Cl2═2Fe3++2Cl-,故C错误;
D.NaHCO3溶液中加入过量的Ba(OH)2溶液的离子反应为HCO3-+Ba2++OH-═BaCO3↓+H2O,故D正确;
故选D.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意离子方程式中保留化学式的物质及电子、电荷守恒,题目难度不大.


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:选择题
| A. | PM2.5是指大气中直径接近于2.5×10-6m(1m=109nm)的颗粒物,也称可吸入颗粒物,这些细颗粒物分散在空气中形成的分散系是胶体 | |
| B. | 胶体的分散质粒子直径小于l00nm但大于1nm,能通过滤纸 | |
| C. | 利用丁达尔效应可以区分溶液和胶体 | |
| D. | 浊液的分散质粒子直径大于l00nm,不能通过滤纸 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X是第IA元素,Y的最高正价是+3价 | |
| B. | Z是周期表中非金属性最强的元素 | |
| C. | 化合物XZ中含有离子键 | |
| D. | Y的单质与X、Z的最高价氧化物的水化物也都能发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉、纤维素、聚乙烯、油脂、蛋白质都是高分子化合物 | |
| B. | 蔗糖和葡萄糖不是同分异构体,但属同系物 | |
| C. | 油酸甘油酯在碱性条件下水解属于皂化反应 | |
| D. | 石油的裂化、裂解属于化学变化,煤的气化、液化则属于物理变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol NaHSO4晶体中含阴阳离子总数是0.3NA | |
| B. | 将0.1mol FeCl3加到沸水中制得的胶体中,含胶粒0.1NA | |
| C. | 1 mol Na2O2与足量H2O完全反应,转移电子数目为2NA | |
| D. | 在常温常压下,13.8g NO2与足量水充分反应,剩余气体的分子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应①中化学能全部转化为热能 | |
| B. | 反应②为吸热反应,在任何情况下都不能自发进行 | |
| C. | 反应③中使用催化剂或移走部分CO,均可提高Fe2O3的转化率 | |
| D. | 反应Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=-28.5 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
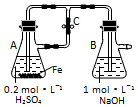
| A. | 用如图装置可以制备沉淀Fe(OH)2 | |
| B. | 提纯含有少量KNO3的NaCl:溶于水,蒸发浓缩、冷却结晶,过滤洗涤干燥 | |
| C. | 检验(NH4)2FeSO4晶体中的NH4+:取样品于试管中溶于水,滴加足量NaOH溶液,加热,将湿润的蓝色石蕊试纸放在试管口,观察试纸是否变红色 | |
| D. | 除去CO2中少量的SO2:可使其通过饱和Na2CO3溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com