
下列实验操作正确的是
A.把试剂瓶中的Na2CO3溶液倒入试管中,发现取量过多,为了不浪费,又把多余的试剂倒入原试剂瓶中
B.分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出
C.先在天平两个托盘上各放一张相同质量的纸,再把氢氧化钠固体放在纸上称
D.萃取碘水中的碘时,可选择苯或酒精作萃取剂
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源:2016届山东省乳山市高三上学期10月月考化学试卷(解析版) 题型:选择题
由锌、铁、铝、镁四种金属中的两种组成的混和物10 g ,与足量的盐酸反应产生的氢气在标准状况下为11.2 L,则混和物中一定含有的金属是
A.锌 B.铁 C.铝 D.镁
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三上期中测试化学试卷(解析版) 题型:实验题
(10分)某小组以CoCl2•6H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X.为确定其组成,进行如下实验。
①氨的测定:精确称取w g X,加适量水溶解,注入如图所示的三颈瓶中,然后逐滴加入足量10%NaOH溶液,通入水蒸气,将样品液中的氨全部蒸出,用V1 mL cl mol•L﹣1的盐酸标准溶液吸收.蒸氨结束后取下接收瓶,用c2 mol•L﹣1NaOH标准溶液滴定过剩的HCl,到终点时消耗V2 mL NaOH溶液.

氨的测定装置(已省略加热和夹持装置)
②氯的测定:准确称取样品X,配成溶液后用AgNO3标准溶液滴定,K2CrO4溶液为指示剂,至出现淡红色沉淀不再消失为终点(Ag2CrO4为砖红色)。
回答下列问题:
(1)装置中安全管的作用原理是________________。
(2)用NaOH标准溶液滴定过剩的HCl时,应使用_____________式滴定管,可使用的指示剂为____________。
(3)样品中氨的质量分数表达式为_____________。
(4)测定氨前应该对装置进行气密性检验,若气密性不好测定结果将__________(填“偏高”或“偏低”)。
(5)测定氯过程中,使用棕色滴定管的原因是_________;滴定终点时,若溶液中c(Ag+)=2.0×10-5 mol•L﹣1,c(CrO42-)为__________mol•L-1。已知:Ksp(Ag2CrO4)=1.12×10-12
(6)经测定,样品X中钴、氨和氯的物质的量之比为1:6:3,钴的化合价__________,制备X的化学方程式为__________;X的制备过程中温度不能过高的原因是__________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年北京大学附属中学分校高二上抽考化学试卷(解析版) 题型:选择题
合成氨反应:N2(g)+3H2(g)  2NH3(g) ΔH =-92.4kJ·mol-1,在反应过程中,正反应速率的变化如下图:
2NH3(g) ΔH =-92.4kJ·mol-1,在反应过程中,正反应速率的变化如下图:
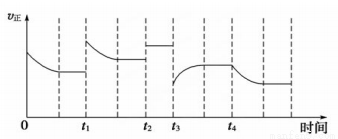
下列说法正确的是
A.t1时升高了温度 B.t2时使用了催化剂
C.t3时增大了压强 D.t4时降低了温度
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁育才学校高一上第一次阶段测化学试卷(解析版) 题型:选择题
标况下,两个容积相同的容器中,一个盛有NH3气体,另一个盛有N2和H2的混合气体。若两容器内的气体具有相等的电子数,则混合气体中N2和H2的物质的量之比为
A.4:1 B.2:1 C. 1:2 D.1:4
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高一上期中测试化学试卷(解析版) 题型:选择题
实验室需配置一种仅含四种离子(不考虑水电离出来的离子)的无色混合溶液,且在混合物溶液中四种离子的浓度均为1mol/L。下列四个选项中能达到此目的的是
A.Na+、K+、SO42-、Cl- B.Cu2+、K+、SO42-、NO3-
C.H+、K+、HCO3-、Cl- D.Mg2+、Na+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁师大附属中学高二10月月考化学试卷(解析版) 题型:选择题
已知反应①:CO(g)+CuO(s) CO2(g)+Cu(s)和反应②:H2(g)+CuO(s)
CO2(g)+Cu(s)和反应②:H2(g)+CuO(s) Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g)
Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g) CO2(g)+H2(g)的平衡常数为K。则下列说法正确的是
CO2(g)+H2(g)的平衡常数为K。则下列说法正确的是
A.反应①的平衡常数K1=
B.反应③的平衡常数K=
C.对于反应③,恒容时,温度升高,H2浓度减小,则该反应的△H>0
D.对于反应③,恒温恒容下,增大压强,H2浓度一定减小
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东寿光中学高一上10月月考化学试卷(解析版) 题型:选择题
下面对氯气的叙述,正确的是
A.液氯可使湿的红布条褪色,所以液氯具有漂白性
B.氯气没有漂白性,但通入品红溶液中,品红褪色
C.在通常情况下,氯气可以和任何金属直接化合
D.氯气有毒,可以用澄清的石灰水尾气吸收;久置的氯水最终变为稀盐酸
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高二上10月月考化学试卷(解析版) 题型:填空题
(16分)下表中实线是元素周期表的部分边界,其中上边界并未用实线标出。
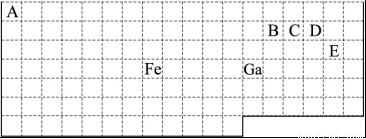
根据信息回答下列问题。
(1)周期表中基态Ga原子的价电子排布式为____________________。
(2)Fe元素位于周期表的____________区;Fe与CO易形成配合物Fe(CO)5,在Fe(CO)5中铁的化合价为_____________;已知:原子数目和电子总数(或价电子总数)相同的微粒互为等电子体,等电子体具有相似的结构特征。与CO分子互为等电子体的分子和离子分别为______________和____________(填化学式)。
(3)在CH4、CO、CH3OH中,碳原子采取sp3杂化的分子有_______________________。
(4)根据VSEPR理论预测 离子的空间构型为_________________。B、C、D、E任意两原子相互化合形成的分子中,所有原子都满足最外层8电子稳定结构的分子的电子式为________________(写2种)。
离子的空间构型为_________________。B、C、D、E任意两原子相互化合形成的分子中,所有原子都满足最外层8电子稳定结构的分子的电子式为________________(写2种)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com