
锌与不同浓度的硝酸反应,HNO3可以被还原成不同价态的产物。下列化学反应中参加反应的锌与被还原的HNO3的物质的量的关系符合图1-12(x表示被还原的HNO3的物质的量,y表示耗去Zn的物质的量)的是( )
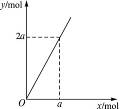
图1-12
A.3Zn+8HNO3(稀)====3Zn(NO3)2+2NO↑+4H2O
B.4Zn+10HNO3(极稀) ====4Zn(NO3)2+NH4NO3+3H2O
C.4Zn+10HNO3(很稀) ====4Zn(NO3)2+N2O↑+5H2O
D.Zn+4HNO3(浓) ====Zn(NO3)2+NO2↑+2H2O
科目:高中化学 来源: 题型:阅读理解
| 硝酸 | 硝酸浓度大于10mol/L | 硝酸浓度为6.6~10mol/L、加热 | 硝酸浓度为6.6~10mol/L |
| 还原产物 | NO2 | NO2 | NO2 |
| 硝酸 | 硝酸浓度为0.1~6.6mol/L、加热 | 硝酸浓度0.1~6.6mol/L | 硝酸浓度0.1mol/L |
| 还原产物 | NO | NO2、N2 | NH4NO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 金属腐蚀造成很大的经济损失,甚至超过自然灾害,其中钢铁锈蚀最为严重,寻求防止钢铁腐蚀的方法意义重大.
金属腐蚀造成很大的经济损失,甚至超过自然灾害,其中钢铁锈蚀最为严重,寻求防止钢铁腐蚀的方法意义重大.| 1 |
| 5 |
| 2 |
| 9 |
| 1 |
| 4 |
| 1 |
| 3 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
金属腐蚀造成很大的经济损失,甚至超过自然灾害,其中钢铁锈蚀最为严重,寻求防止钢铁腐蚀的方法意义重大。
⑴钢铁的表面发蓝、发黑处理是常用的防腐方法。下列反应是主要反应之一。
请配平化学方程式:
口Na2FeO2+ 口NaNO2+ 口 =口 NaFeO2+ 口NH3↑+ 口NaOH
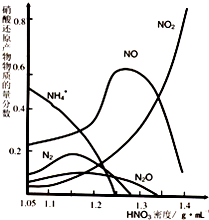
⑵钢铁的“钝化”处理也能达到防腐目的,经冷、浓HNO3处理后,其表面有一层致密氧化物保护膜,但是加热或在稀HNO3中就不能“钝化”。不同浓度的HNO3与铁反应的还原产物很复杂,其分布曲线如图。

①图示可知,密度大于1.35 g?mL-1的硝酸与铁反应时,其还原产物主要是 ;密度为1.05g?mL-1 的硝酸与铁反应时,其最多的还原产物是 ;分析HNO3与铁反应的规律是 。
②工业上一般不用冷浓硝酸进行铁表面处理,其可能的原因是: 。
⑶金属 (M) 的腐蚀是因为发生反应: M-ne-→Mn+。钢铁除了上述表面处理的方法外,下列方法也能起到防腐作用的是 (填字母编号)。
A.在铁中掺入铬、镍等金属,改变其内部结构,制成不锈钢
B.在铁制品表面镀锌
C.提高铁中含碳量,制成生铁
D.将水库铁闸门与直流电源的负极相连
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:
较活泼的金属锌与不同浓度的硝酸反应时,可得到不同价态的还原产物,如果其反应的锌和被还原的硝酸的物质的量之比为4:1,则硝酸的还原产物可能是
A.NO2 B.NO C.N2O D.NH4NO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com