
【题目】氯化铵具有广泛用途,可用于选矿、医药等。
(1)实验室用氯化铵与熟石灰反应制取氨气的化学方程式为____,收集氨气时,可选用下图中的装置____(填字母)。
A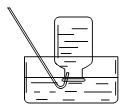 B
B C
C![]()
(2)工业上为提高氯化铵产品的经济利用价值,常利用氢氧化镁和氯化铵共热制得氨气、碱式氯化镁[Mg(OH)Cl](520℃发生分解)。实验室模拟该工艺的装置图如下:

①冷凝管进水口是_____(填“a”或“b”)。
②实验中持续通入氮气的目的是_____。
③共热时,温度不宜过高的原因是_____。
④共热时,若氯化铵用量过大会导致Mg(OH)Cl中混有较多的杂质为_____(写化学式)。
(3)已知氧化钙与氯化铵溶液反应制备氯化钙的适宜温度为80℃。补充完整由氧化钙(含少量SiO2)、氯化铵溶液制备医用CaCl2·2H2O晶体的实验步骤:将氯化铵溶液、氧化钙粉末按照一定配比加入反应器中,_____,得到CaCl2溶液,_____、趁热过滤、洗涤、干燥。(实验中须使用的试剂:稀硫酸)
【答案】Ca(OH)2+2NH4Cl![]() CaCl2+2NH3↑+2H2O B b 使装置内的NH3尽量排出 Mg(OH)Cl温度高时会分解 MgCl2 80℃水浴加热并不断搅拌,用硫酸溶液吸收蒸出的氨气,充分反应后过滤 将滤液蒸发结晶
CaCl2+2NH3↑+2H2O B b 使装置内的NH3尽量排出 Mg(OH)Cl温度高时会分解 MgCl2 80℃水浴加热并不断搅拌,用硫酸溶液吸收蒸出的氨气,充分反应后过滤 将滤液蒸发结晶
【解析】
⑴实验室用氯化铵与熟石灰反应制取氨气的化学方程式为Ca(OH)2+2NH4Cl![]() CaCl2+2NH3↑+2H2O,氨气极易溶于水且密度比空气小,因此只能采用向下排空气法收集,只能用装置B来收集氨气,
CaCl2+2NH3↑+2H2O,氨气极易溶于水且密度比空气小,因此只能采用向下排空气法收集,只能用装置B来收集氨气,
故答案为:Ca(OH)2+2NH4Cl![]() CaCl2+2NH3↑+2H2O;B;
CaCl2+2NH3↑+2H2O;B;
⑵

①冷凝管进水口应下进上出,因此进口管是b,
故答案为b;
②实验中持续通入氮气的目的是使装置内的NH3尽量排出;
③共热时,根据信息Mg(OH)Cl在520℃发生分解,因此温度不宜过高的原因是Mg(OH)Cl温度高时会分解,
故答案为:Mg(OH)Cl温度高时会分解;
④共热时,若氯化铵用量过大,两者按照2:1反应生成氯化镁,因此用量过大会导致Mg(OH)Cl中混有较多的杂质MgCl2,
故答案为:MgCl2;
⑶已知氧化钙与氯化铵溶液反应制备氯化钙的适宜温度为80℃。所以由氧化钙(含少量SiO2)、氯化铵溶液制备医用CaCl2·2H2O晶体的实验步骤为:将氯化铵溶液、氧化钙粉末按照一定配比加入反应器中,控制水浴温度为80℃加热并不断搅拌,发生反应Ca(OH)2+2NH4Cl![]() CaCl2+2NH3↑+2H2O,用硫酸溶液吸收蒸出的氨气,由于氧化钙中含有二氧化硅杂质,因此将反应后的溶液先过滤除去二氧化硅,再加热蒸发结晶、趁热过滤出氯化钙、洗涤、干燥。
CaCl2+2NH3↑+2H2O,用硫酸溶液吸收蒸出的氨气,由于氧化钙中含有二氧化硅杂质,因此将反应后的溶液先过滤除去二氧化硅,再加热蒸发结晶、趁热过滤出氯化钙、洗涤、干燥。
故答案为:80℃水浴加热并不断搅拌,用硫酸溶液吸收蒸出的氨气,充分反应后过滤;将滤液蒸发结晶。


科目:高中化学 来源: 题型:
【题目】某校学生用中和滴定法测定某NaOH溶液的物质的量浓度,选甲基橙作指示剂。
(1)配制250mL 0.2000 mol/L盐酸标准溶液,所需玻璃仪器有______、______量筒、烧杯、玻璃棒。
(2)盛装0.2000 mol/L盐酸标准液应该用______式滴定管。(填“酸”或“碱”)
(3)滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视_________,直到加入一滴盐酸后,溶液由_________,即到终点。
(4)滴定操作可分解为如下几步:
①检查滴定管是否漏水;
②取一定体积的待测液于锥形瓶中;
③用标准溶液润洗盛标准溶液的滴定管,用待测液润洗盛待测液的滴定管;
④装标准溶液和待测液并调整液面(记录初始读数);
⑤用蒸馏水洗涤玻璃仪器;⑥滴定操作
正确的操作顺序为:_________。
(5)有关数据记录如下:
实验序号 | 待测液体积(mL) | 所消耗盐酸标准液的体积(mL) | |
滴定前 | 滴定后 | ||
1 | 20.00 | 0.60 | 20.70 |
2 | 20.00 | 6.00 | 25.90 |
3 | 20.00 | 1.40 | 23.20 |
则NaOH溶液的物质的量浓度为__________mol/L。
(6)若滴定时锥形瓶未干燥,则测定结果____________;若滴定前平视读数,滴定终点时仰视读数,则所测碱的浓度值_________。(填“无影响”、“偏高”或“偏低”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在高温下一氧化碳可将二氧化硫还原为单质硫。已知:
C(s)+O2(g)=CO2(g) H1=-393.5kJ·mol-1
CO2(g)+C(s)=2CO(g) H2=+172.5kJ·mol-1
S(s)+O2(g)=SO2(g) H3=-296.0kJ·mol-1
写出CO除SO2的热化学方程式_______。
(2)某同学想利用下图装置验证同主族元素非金属性的变化规律。
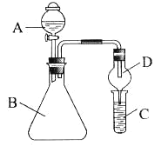
①若要证明非金属性Cl>I,则在A 中加浓盐酸,B中加KMnO4固体,C中加入淀粉碘化钾溶液,观察到C中溶液_____的现象,即可证明。从环境保护的观点考虑,此装置的缺点是_____。
②若要证明非金属性C>Si,则在A 中加盐酸,B中加CaCO3固体,C中加_____(写化学式)溶液。该同学认为若观察到C中溶液有白色沉淀生成,即可证明,该方案存在明显缺陷,可通过在两装置间添加装有_____溶液的洗气瓶进行改进。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)肼(N2H4)分子可视为NH3分子中的一个氢原子被—NH2(氨基)取代形成的另一种氮的氢化物。
①肼可用作火箭燃料,燃烧时发生的反应是:N2O4(l)+2N2H4(l)=3N2(g)+4H2O(g) ΔH=-1038.7 kJ·mol-1,若该反应中有4 mol N—H键断裂,则形成的π键有________mol。
②肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4晶体内不存在___(填标号)。
a.离子键 b.共价键 c.配位键 d.范德华力
(2)ⅥA族元素氧、硫、硒(Se)的化合物在研究和生产中有许多重要用途。请回答:
①H2Se的酸性比H2S________(填“强”或“弱”),SO32-离子的立体构型为________。
②H2SeO3的K1和K2分别为2.7×10-3和2.5×10-8,H2SeO4第一步几乎完全电离,K2为1.2×10-2,请根据结构与性质的关系解释:H2SeO4比H2SeO3酸性强的原因:__________。
(3)[Zn(CN)4]2-在水溶液中与HCHO发生如下反应:4HCHO+[Zn(CN)4]2-+4H++4H2O=[Zn(H2O)4]2++4HOCH2CN
①Zn2+基态核外电子排布式为___________________。
②与H2O分子互为等电子体的阴离子为________。
③)[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键。不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在日常生活和生产过程中化学有着重要的应用,下列有关说法正确的是![]()
A.洪涝、地震灾区灾后常用石灰对环境进行消毒,是利用石灰可使蛋白质变性的性质
B.食品添加剂对人体均有益,因此在添加时无需对其用量进行严格控制
C.生活中常见的石英玻璃、普通玻璃、钢化玻璃都属于硅酸盐产品
D.根据分散系的稳定性,将分散系分为溶液、胶体和浊液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1mol有机物X最多能与1 mol HCl发生加成反应得到Y,1 mol Y能与4 mol Cl2在一定条件下发生取代反应得到Z。已知Y分子中的碳碳键都是单键,Z分子中没有氢原子,则X的结构简式可能是( )
A.![]() B.CH≡CH
B.CH≡CH
C.![]() D.CH≡CCH3
D.CH≡CCH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用光伏电池提供电能处理废水中的污染物(有机酸阴离子用R-表示),并回收有机酸HR,装置如图所示。下列说法错误的是
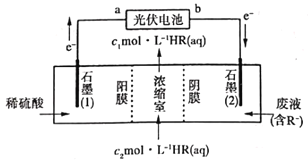
A.在光伏电池中a极为正极B.石墨(2)极附近溶液的pH降低
C.HR溶液:c2<c1D.若两极共收集3mol气体,则理论上转移4mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A.CaCl2溶液中通入CO2:Ca2++CO2+H2O===CaCO3↓+2H+
B.向硫酸铝溶液中滴加碳酸钠溶液:2Al3++3CO32=Al2(CO3)3↓
C.NH3通入NaClO溶液中被氧化成N2:3ClO-+2NH3===N2+3Cl-+3H2O
D.向 NH4Al(SO4)2溶液中加入Ba(OH)2溶液至SO42-恰好沉淀完全:Al3++2SO42-+2Ba2++3OH-=Al(OH)3↓+2BaSO4↓
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com