
| 136×0.235 |
| 16 |
| 104 |
| 12 |
 .
.| 136×0.235 |
| 16 |
| 104 |
| 12 |
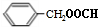 、
、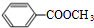 、
、 ,
,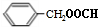 、
、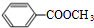 、
、 ;
;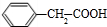 +NaHCO3→
+NaHCO3→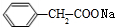 +CO2↑+H2O,
+CO2↑+H2O,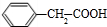 +NaHCO3→
+NaHCO3→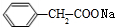 +CO2↑+H2O;
+CO2↑+H2O; ,其银镜反应方程式为:
,其银镜反应方程式为: +2Ag(NH3)2OH
+2Ag(NH3)2OH| △ |
 +2Ag↓+3NH3+H2O,
+2Ag↓+3NH3+H2O, +2Ag(NH3)2OH
+2Ag(NH3)2OH| △ |
 +2Ag↓+3NH3+H2O.
+2Ag↓+3NH3+H2O.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、生成的水分子中含有18O |
| B、生成的乙酸乙酯中含有18O |
| C、可能生成88g乙酸乙酯 |
| D、不可能生成90g乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 25.00 | 0.00 | 20.30 |
| 第二次 | 25.00 | 0.00 | 20.20 |
| 第三次 | 25.00 | 4.00 | 24.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X中一定不存在FeO |
| B、不容物Y中一定含有FeO和CuO |
| C、Z溶液中一定存在K2CO3 |
| D、Y中一定存在MnO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 实验数据1 | 实验数据2 | 实验数据3 | |
| 甲小组 | 反应前氧化铜的质量为m1g | 氧化铜反应后剩余固体的质量为m2g | 生成氮气在标准状况下的体积为V1L |
| 乙小组 | 洗气前装置D的质量为m3g | 洗气后装置D的质量为m4g | 生成氮气在标准状况下的体积为V2L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④⑤ |
| B、②③⑤④① |
| C、⑤①②③④ |
| D、⑤③②①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用过滤的方法除去食盐中的泥沙 |
| B、用分液的方法分离汽油和水 |
| C、用结晶的方法分离氯化钠和硝酸钾 |
| D、用加热的方法除去碳酸氢钠中混有的碘 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用银氨溶液鉴别HCOOCH3和CH3CHO |
| B、用溴水鉴别乙烯和乙炔 |
| C、用核磁共振氢谱鉴别1-溴丙烷和2-溴丙烷 |
| D、用KMnO4酸性溶液鉴别CH3CH=CHCH2OH和CH3CH2CH2CHO |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com