
| A. | pH=2的溶液 | B. | c(OH)=1×10-13mol/L | ||
| C. | c(H+)=1×10-5mol/L | D. | c(H2SO4)=0.75mol/L |
科目:高中化学 来源: 题型:选择题
| A. | 一水合氨的电离方程式:NH3•H2O?NH4++OH- | |
| B. | 氯化镁的摩尔质量:95g | |
| C. | 亚硫酸的化学式:H2SO3 | |
| D. | Na+的结构示意图: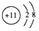 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在通常状况下,氧的单质为气体,硫的单质为固体 | |
| B. | 氢硫酸溶液在空气中置露会变浑浊 | |
| C. | 硫化氢在加热的条件下可分解成氢气和硫,而水在强高温时很少分解 | |
| D. | 铜与硫反应生成硫化亚铜,与氧气反应生成氧化铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $C=\frac{1000m}{VM}$ | B. | $C=\frac{1000ρW}{M}$ | C. | $W%=\frac{CM}{1000ρ}$ | D. | $m=\frac{VρW}{1000}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通过酸性KMnO4后再通过澄清石灰水 | |
| B. | 通过Ba(OH)2溶液再通过石灰水 | |
| C. | 直接通过澄清石灰水 | |
| D. | 通过小苏打悬浊液再通过石灰水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KMnO4 | B. | H2O2 | C. | Cl2 水 | D. | HNO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com