
| 离子化合物 | AB | CD | EF |
| 离子电荷数 | 1 | 1 | 2 |
| 键长(10-10m) | 2.31 | 3. 18 | 2.10 |
科目:高中化学 来源:不详 题型:单选题
A.Z的电子式为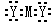 | B.Z可表示为M2Y |
| C.Z一定溶于水中 | D.M形成+2价阳离子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2(ax+by)+60 | B.ax+by+60 | C.(ax+by)/2+60 | D.ay+bx+60 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| | 水 | 四氯化碳 |
| 溴 | 黄→棕 | 橙→橙红 |
| 碘 | 深黄→褐 | 紫→深紫 |
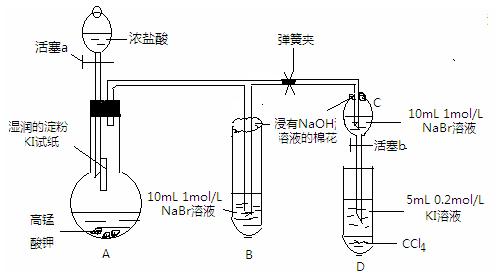
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.硫酸盐的化学式为R2SO4,它易溶于水 |
| B.单质与水剧烈反应甚至发生爆炸 |
| C.R的最高价氧化物对应的水化物的碱性强于氢氧化钠 |
| D.在同族的单质中R的单质熔点最高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 粒子代码 | X | Y | Z |
| 原子核数 | 单核 | 两核 | 四核 |
| 粒子的电荷数 | 一个单位正电荷 | 一个单位负电荷 | 0 |


查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com