
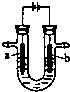
| A.a为正极,b为负极 | B.a极上有氢气放出 |
| C.b极上发生氧化反应 | D.b极附近溶液显碱性 |
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源:不详 题型:单选题
| A.把铁片与电源的正极相连 |
| B.电解质必须用含有锌离子的可溶性盐 |
| C.锌极发生氧化反应 |
D.铁极的电极反应式为Zn2++2e- Zn Zn |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
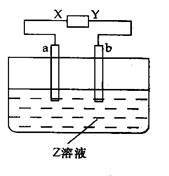
| | a极板 | b极板 | x极板 | 溶质 |
| A | 锌 | 石墨 | 负极 | CuSO4 |
| B | 石墨 | 石墨 | 负极 | NaOH |
| C | 银 | 铁 | 正极 | AgNO3 |
| D | 铜 | 石墨 | 负极 | CuCl2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| ||
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
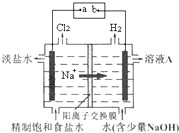
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.64.7% | B.47.5% | C.32.2% | D.28.3% |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
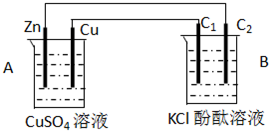
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com