
【题目】A、B、C、D四种有机物分子中的碳原子数目相同,标准状况下烃A对氢气的相对密度是13;烃B跟HBr反应生成C;C与D混合后加入NaOH并加热,可生成B。
(1)写出有机物的结构简式:A____;D____。
(2)写出有关反应的化学方程式:____。
【答案】CH![]() CH CH3CH2OH CH2=CH2 + HBr
CH CH3CH2OH CH2=CH2 + HBr ![]() CH3CH2Br,CH3CH2Br + NaOH
CH3CH2Br,CH3CH2Br + NaOH![]() CH2=CH2↑+ NaBr + H2O
CH2=CH2↑+ NaBr + H2O
【解析】
A、B、C、D四种有机物分子中的碳原子数目相同,标准状况下烃A对氢气的相对密度是13,则A的摩尔质量为![]() ,则M=26gmol-1,A的相对分子质量为26,除以12得到碳的原子数目和氢原子数目,因此A的分子式为C2H2,烃B跟HBr反应生成C,因此B为C2H4,为乙烯CH2=CH2,则C为CH3CH2Br,C与D混合后加入NaOH并加热,可生成B,C发生消去反应,D为乙醇CH3CH2OH。
,则M=26gmol-1,A的相对分子质量为26,除以12得到碳的原子数目和氢原子数目,因此A的分子式为C2H2,烃B跟HBr反应生成C,因此B为C2H4,为乙烯CH2=CH2,则C为CH3CH2Br,C与D混合后加入NaOH并加热,可生成B,C发生消去反应,D为乙醇CH3CH2OH。
(1)根据上面分析得出有机物的结构简式:A.CH![]() CH;D. CH3CH2OH,故答案为:CH
CH;D. CH3CH2OH,故答案为:CH![]() CH;CH3CH2OH。
CH;CH3CH2OH。
(2)写出有关反应的化学方程式:CH2=CH2 + HBr ![]() CH3CH2Br,CH3CH2Br + NaOH
CH3CH2Br,CH3CH2Br + NaOH![]() CH2=CH2↑+ NaBr + H2O,故答案为:CH2=CH2 + HBr
CH2=CH2↑+ NaBr + H2O,故答案为:CH2=CH2 + HBr ![]() CH3CH2Br;CH3CH2Br + NaOH
CH3CH2Br;CH3CH2Br + NaOH![]() CH2=CH2↑+ NaBr + H2O。
CH2=CH2↑+ NaBr + H2O。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知SO2可以用Fe(NO3)3溶液吸收,按如图所示装置展开相关探究:取一定量的铜片于三颈烧瓶中,通入一段时间N2后再加入足量的浓硫酸,加热;装置A中有白雾(硫酸酸雾)生成,装置B中产生白色沉淀。回答下列问题:
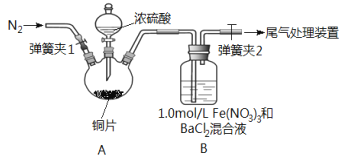
(1)装置A中用于添加浓硫酸的仪器名称为_________________。
(2)实验开始前需进行的操作是_____________________。
(3)加入浓硫酸之前先通入N2一段时间,其目的是_____________。
(4)排除装置A中白雾影响,可在装置A、B间增加洗气瓶C,则C中盛放的试剂是_______;若用NaOH溶液处理尾气,则发生反应的离子方程式为__________。
(5)经过讨论,该小组对装置B中产生沉淀的原因,提出下列假设(不考虑各因素的叠加,不考虑体系残留的氧气);
假设1:装置A中白雾进入装置B中参与了反应;
假设2:________;
假设3: Fe(NO3)3溶液显酸性,在此酸性条件下NO3-能氧化SO2。
(6)请你设计实验验证上述假设3,写出实验步骤、预期现象和结论。
实验步骤(简述操作过程) | 预期现象和结论 |
①测1.0mol/LFe(NO3)3溶液的pH ②取与Fe(NO3)3溶液中c(NO3-)相同的适量Ba(NO3)2溶液滴入试管中 ③______________ ④向试管中通入适量SO2气体 | _____________ |
(7)若假设2正确,请写出B中发生氧化还原反应的离子方程式:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验不能达到目的的是( )
选项 | 目的 | 实验 |
A | 制取较高浓度的次氯酸溶液 | 将Cl2通入小苏打溶液中 |
B | 除去溴苯中的少量溴 | 加入苛性钠溶液洗涤、分液 |
C | 加快氢气的生成速率 | 将与稀硫酸反应的粗锌改为纯锌 |
D | 制备少量氨气 | 向新制生石灰中滴加浓氨水 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列混合物中可用分液漏斗分离,且有机物应从分液漏斗上口倒出的是 ( )
A.![]() 、Br2
、Br2
B.CH3Cl、H2O
C.CCl4、CHCl3
D.CH2Br—CH2Br、NaBr(H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烯烃A在一定条件下可以按框图进行反应:

已知:①D是
②F1和F2互为同分异构体
③G1和G2互为同分异构体
根据框图信息,填写下列空白:
(1)A的结构简式是____。
(2)框图中属于取代反应的是(填数字代号):____。
(3)框图中①、③、⑥属于____反应。
(4)G1的结构简式是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
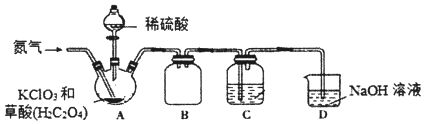
【题目】二氧化氯(C1O2)是一种黄绿色气体,沸点为11℃,不稳定,在混合气体中的体积分数大于10%就可能发生爆炸,在工业上常用作水处理剂、漂白剂。C1O2易溶于水但不与水反应,其水溶液在温度过高时有可能爆炸。某小组按照以下实验装置制备C1O2并验证其某些性质。
请回答下列问题:
(1)实验时A装置需要控制温度为60~80℃,则A装置加热的方式是___,该加热方式的优点是_____。
(2)通入氨气的主要作用有两个,一是可以起到搅拌作用,二是____。
(3)B装置的作用是___。C装置用来吸收C1O2,则C中液体易选用下列___(填序号)。
①热水 ②冰水 ③饱和食盐水
(4)装置D中C1O2与NaOH溶液反应可生成等物质的量的两种钠盐,其中一种为NaClO2,装置C中生成这两种钠盐的化学方程式为____。饱和NaClO2溶液在温度低于38℃时析出晶体NaC1O23H2O,在温度高于38℃时析出晶体NaClO2.请补充从NaClO2溶液中制得NaClO2晶体的操作步骤:a.___;b.___;c.洗涤;d.干燥。
(5)设计一个简易实验证明二氧化氯具有永久的漂白性:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设 NA为阿伏加德罗常数的值,下列说法不正确的是
A.2 mol SO2 和 1 mol O2 混合在 V2O5 存在的条件下于密闭容器中加热反应后,容器内物质分子数大于2NA
B.某温度下纯水的 pH=6,该温度下 1L pH=11 的NaOH 溶液中含OH-的数目为 0.1NA
C.一定温度下,1 L 0.5 mol·L -1 NH4Cl 溶液与 2 L 0.25 mol·L -1NH4Cl 溶液含NH+均为 0.5NA
D.100 g CaCO3 与 KHCO3 的混合物中含有的阴离子的数目为 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环丁基甲酸是有机合成中一种有用的中间体。某研究小组以丙烯醛为原料,设计了如下路线合成环丁基甲酸。


请回答:
(1)化合物C的结构简式是 __________________。
(2)下列说法中不正确的是__________________ 。
A.化合物A能与NaHCO3溶液反应
B.化合物B和C能形成高聚物
C.化合物G的化学式为C6H8O4
D.1 mol化合物B与足量金属钠反应能生成1 mol氢气
(3)写出D + E → F的化学方程式:__________________。
(4)环丁基甲酸与苯酚反应生成一种酯X,写出化合物X满足下列条件的所有同分异构体的结构
简式:__________________
① 能使FeCl3溶液变紫色;
② 含有丙烯醛中所有的官能团;
③ 1H-NMR谱显示分子中含有5种不同化学环境的氢原子。
(5) 以1,3-丁二烯和E为原料可制备环戊基甲酸(![]() ),请你选用必要试剂,设计该合成路线。__________________
),请你选用必要试剂,设计该合成路线。__________________
查看答案和解析>>
科目:高中化学 来源: 题型:
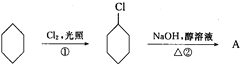
【题目】从环己烷可制备1,4-环己二醇,合成步骤如下。试回答:
![]()
![]()
(1)反应①反应类型属于____。
(2)羟基的电子式____。
(3)化合物的结构简式:B____,C_____。
(4)完成以下步骤方程式(注明反应条件)④____。
(5)反应⑤中可能产生一定量的副产物,任写一个其可能的结构简式为___。
(6)反应⑥所用试剂和条件是___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com