
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是: I1=738kJ/mol I2=1451kJ/mol I3=7733kJ/mol I4=10540kJ/mol |
| D原子核外所有p轨道全满或半满 E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 G在周期表的第七列 |
 ,该同学所画的电子排布图违背了泡利不相容原理
,该同学所画的电子排布图违背了泡利不相容原理分析 A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大,
A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素,A为H元素;
B元素原子的核外p电子数比s电子数少1,B有2个电子层,核外电子排布为1s22s22p3,故B为N元素;
由C原子的第一至第四电离能数据可知,第三电离能剧增,故C表现+2价,处于ⅡA族,原子序数大于N元素,故C为Mg元素;
D处于第三周期,D原子核外所有p轨道全满或半满,最外层排布为3s23p3,故D为P元素;
E处于第三周期,E元素的主族序数与周期数的差为4,E处于第ⅦA族,故E为Cl元素;
F是前四周期中电负性最小的元素,金属性最强,F为第四周期元素,故F为K元素,
G处于第四周期,且在周期表的第7列,G为Mn元素.
解答 解:A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大,
A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素,A为H元素;
B元素原子的核外p电子数比s电子数少1,B有2个电子层,核外电子排布为1s22s22p3,故B为N元素;
由C原子的第一至第四电离能数据可知,第三电离能剧增,故C表现+2价,处于ⅡA族,原子序数大于N元素,故C为Mg元素;
D处于第三周期,D原子核外所有p轨道全满或半满,最外层排布为3s23p3,故D为P元素;
E处于第三周期,E元素的主族序数与周期数的差为4,E处于第ⅦA族,故E为Cl元素;
F是前四周期中电负性最小的元素,金属性最强,F为第四周期元素,故F为K元素,
G处于第四周期,且在周期表的第7列,G为Mn元素.
(1)B为N元素,核外电子排布为1s22s22p3,基态原子中能量最高的电子,处于2p能级,其电子云在空间有3个方向,原子轨道呈纺锤形,
故答案为:2p;3;纺锤;
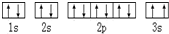
(2)某同学根据上述信息,推断C基态原子的核外电子排布为 ,3s能级2个电子自旋方向相同,该同学所画的电子排布图违背了:泡利不相容原理,
,3s能级2个电子自旋方向相同,该同学所画的电子排布图违背了:泡利不相容原理,
故答案为:泡利不相容原理;
(3)G为Mn元素,是25号元素,位于第四周期第ⅦB族,最后填充的为d电子,为d区元素,价电子排布式为3d54s2,
故答案为:ⅦB;d;3d54s2;
(4)PCl3中心原子P原子价层电子对是为3+$\frac{5-1×3}{2}$=4,含有1对孤对电子对,杂化轨道数为4,杂化方式为sp3,其空间构型为三角锥形,
故答案为:sp3;三角锥形;
(5)(SCN)2的结构式为N≡C-S-S-C≡N,根据[(SCN)2]的结构可知分子中有3个单键和2个碳氮三键,单键为σ键,三键含有1个σ键、2个π键,(SCN)2分子含有5个σ键,故1mol(SCN)2分子中含有σ键的数目为 5NA,
由于异硫氰酸分子间可形成氢键,而硫氰酸分子间不能形成氢键,所以硫氰酸(H-S-C≡N)的沸点低于异硫氰酸,
故答案为:5NA;异硫氰酸分子间可形成氢键,而硫氰酸分子间不能形成氢键;
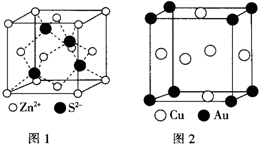
(6)由图可知,S2-离子周围有4个Zn2+,S2-的配位数为4,
故答案为:4;
(7)晶胞中Cu原子数目为6×$\frac{1}{2}$=3、Au原子数目为8×$\frac{1}{8}$=1,晶胞质量为$\frac{3×64+197}{{N}_{A}}$g,晶胞边长为a nm,则晶胞体积为(a×10-7 cm)3,该金属互化物的密度为$\frac{3×64+197}{{N}_{A}}$g÷(a×10-7 cm)3=$\frac{389}{{N}_{A}×{a}^{3}×1{0}^{-21}}$g•cm-3,
故答案为:$\frac{389}{{N}_{A}×{a}^{3}×1{0}^{-21}}$.
点评 本题是对物质结构的考查,涉及核外电子排布、电子云、杂化轨道、分子结构、化学键、氢键、晶胞计算等,题目综合性较大,推断元素是解题的关键,注意基础知识的掌握,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 元素A、B组成的化合物常温下一定呈气态 | |
| B. | 元素C、D的最高价氧化物对应的水化物之间不能发生反应 | |
| C. | 工业上常用电解法制备元素C、D、E的单质 | |
| D. | 化合物AE与CE有相同类型的化学键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N5+中氮-氮之间是以共价键结合 | B. | N5+具有35个电子 | ||
| C. | 化合物N5AsF6中As的化合价为+5 | D. | 化合物N5AsF6中F的化合价为-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X原子核外有16个电子 | |
| B. | XO32-有42个质子 | |
| C. | X的氧化物对应的水化物是一种强酸 | |
| D. | X为金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③②④ | B. | ③④②① | C. | ①③④② | D. | ③①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该化合物仅含碳、氢两种元素 | B. | 该化合物中碳、氢原子个数比为1:2 | ||
| C. | 无法确定该化合物是否含有氧元素 | D. | 该化合物中一定含有氧元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电池的电解液为碱性溶液,负极为Fe | |
| B. | 电池放电过程中,负极附近溶液的pH降低 | |
| C. | 电池放电时,若外电路中有2mol电子转移,则内电路中有2molOH-移向正极 | |
| D. | 电池放电时,负极反应为Fe+2OH--2e-═Fe(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①③⑤ | C. | 全部 | D. | 都不是 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com