
| A£® | NaHCO3 | B£® | FeSO4 | C£® | FeCl3 | D£® | Na2CO3 |
·ÖĪö ¼ÓČČÕōøɲ¢×ĘÉյĹż³ĢÖŠ£¬ŅŖ×¢Ņāæ¼ĀĒŃĪµÄĖ®½āĘ½ŗāµÄŅĘ¶Æ”¢ĪļÖŹµÄŃõ»Æ”¢ĪļÖŹµÄ·Ö½āµČĒéæö£¬ĀČ»ÆĀĮŅ×Ė®½ā£¬Ģ¼ĖįĒāĆ¾¼ÓČČŅ×·Ö½ā£¬ĮņĖįŃĒĢśŅ×±»Ńõ»Æ£®
½ā“š ½ā£ŗA£®Ģ¼ĖįĒāÄĘŹÜČČ·Ö½āÉś³ÉĢ¼ĖįÄĘ”¢¶žŃõ»ÆĢ¼ŗĶĖ®£¬¹ŹA“ķĪó£»
B£®ĮņĖįŃĒĢśČÜŅŗŌŚ¼ÓČČ¹ż³ĢÖŠŅ×±»Ńõ»Æ£¬¹ŹB“ķĪó£»
C£®FeCl3ČÜŅŗ¼ÓČČŹ±Ė®½āÉś³ÉĒāŃõ»ÆĢśŗĶŃĪĖį£¬ŃĪĖįŅ×»Ó·¢£¬Éś³ÉµÄĒāŃõ»ÆĢśŌŚ×ĘÉÕŹ±Éś³ÉŃõ»ÆĢś£¬¹ŹC“ķĪó£»
D£®Ģ¼ĖįÄĘŌŚČÜŅŗŌŚ¼ÓČČŹ±Ė®½āµĆµ½Ģ¼ĖįĒāÄĘÓėĒāŃõ»ÆÄĘ£¬µ«ĒāŃõ»ÆÄĘÄѻӷ¢£¬×īŗóµĆµ½µÄ¹ĢĢåĪŖNa2CO3£¬¹ŹDÕżČ·£®
¹ŹŃ”D£®
µćĘĄ ±¾Ģā×ŪŗĻæ¼²éĪļÖŹµÄŠŌÖŹ£¬²ąÖŲÓŚĖ®½ā”¢·Ö½āµČÖŖŹ¶£¬ĪŖøßĘµæ¼µć£¬ĢāÄæÄŃ¶Č²»“ó£¬×¢ŅāĻą¹ŲĪļÖŹµÄŠŌÖŹµÄÕĘĪÕ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | HCl | B£® | NaOH | C£® | CuSO4 | D£® | KNO3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 2£¬4£¬4-Čż¼×»ł¼ŗĶ飬
2£¬4£¬4-Čż¼×»ł¼ŗĶ飬 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | °×“× | B£® | Ź³ÓĆÓĶ | C£® | Ź³ŃĪ | D£® | ¾Ę¾« |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
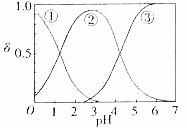 ²ŻĖį”¢²ŻĖįŃĪŌŚ¹¤ŅµÉś²śÉĻÓĆĶ¾·Ē³£¹ć·ŗ£¬H2C2O4Ė®ČÜŅŗÖŠH2C2O4”¢HC2O4ŗĶC2O${\;}_{4}^{2-}$ČżÖÖŠĪĢ¬µÄĮ£×ӵķֲ¼·ÖŹż¦ÄĖęČÜŅŗpH±ä»ÆµÄ¹ŲĻµČēĶ¼ĖłŹ¾£®
²ŻĖį”¢²ŻĖįŃĪŌŚ¹¤ŅµÉś²śÉĻÓĆĶ¾·Ē³£¹ć·ŗ£¬H2C2O4Ė®ČÜŅŗÖŠH2C2O4”¢HC2O4ŗĶC2O${\;}_{4}^{2-}$ČżÖÖŠĪĢ¬µÄĮ£×ӵķֲ¼·ÖŹż¦ÄĖęČÜŅŗpH±ä»ÆµÄ¹ŲĻµČēĶ¼ĖłŹ¾£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
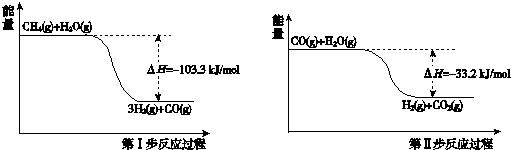
| ĘšŹ¼ÅØ¶Č | ¼× | ŅŅ | ±ū |
| c£ØH2O£©/mol/L | 0.010 | 0.020 | 0.020 |
| c£ØCO£©/mol/L | 0.010 | 0.010 | 0.020 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ū | B£® | ¢Ś¢Ü | C£® | ¢Ū¢Ü | D£® | ¢Ł¢Ś |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com