

图5-3
(1)指出装置中存在的错误:_____________________________________________。
(2)在反应器中发生的化学反应是__________________________________________。
(3)反应中浓硫酸的作用是______________________________________________。
(4)在加热时,应注意使温度迅速升到170 ℃的理由是:__________________。
(5)在烧瓶中加入少量碎瓷片的作用是__________________________________________。
(6)反应中常有少量的副产物SO2生成,SO2对乙烯的性质实验有无影响_______(填“有”或“无”),试叙述除去SO2的方法__________________________。
(7)实验室里,常用_______的方法收集乙烯气体。反应完毕后,应先_______再_______。
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
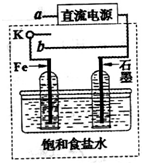 (2013?淄博二模)海水是丰富的资源宝库,从海水中提取元素是化学工业的重要组成部分.
(2013?淄博二模)海水是丰富的资源宝库,从海水中提取元素是化学工业的重要组成部分.查看答案和解析>>
科目:高中化学 来源: 题型:
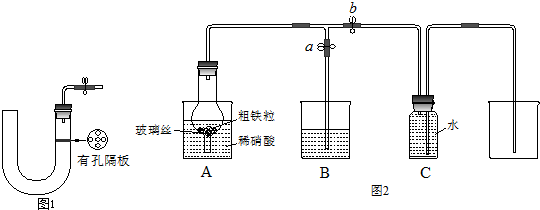
 如图是某同学设计的放热反应的观察装置.其实验顺序是:
如图是某同学设计的放热反应的观察装置.其实验顺序是:查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 高温 |
| 实验步骤 | 操作 | 现象与结论 |
| 第一步 | 取少量液体装于试管,向试 管中滴入几滴KSCN溶液. |
|
| 第二步 | 若溶液紫色褪去,则说明含有Fe2+; 若无明显变化,则说明不含Fe2+. |
查看答案和解析>>
科目:高中化学 来源: 题型:
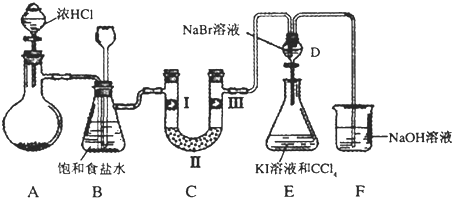
| a | b | c | d | |
| I | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| II | 碱石灰 | 硅胶 | 碱石灰 | 无水氯化钙 |
| III | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com