
使一定量锌与100 mL 18.5 mol·L-1浓H2SO4充分反应,锌完全溶解,同时生成标准状况下气体33.6 L。将反应后溶液稀释,测得其pH=1.0。
求: (1)生成气体的成分及体积(假设浓H2SO4与Zn反应还原产物只生成SO2);
(2)锌的质量;
(3)开始生成H2时H2SO4的浓度(假设溶液体积无变化)。
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案科目:高中化学 来源:2012-2013学年浙江省宁海县正学中学高一下学期第一次阶段性测试化学试卷(带解析) 题型:填空题
(1)在试管里放入一小块铜片,注入一定体积的浓硫酸,给试管加热,使之反应。若铜片还有剩余硫酸是否消耗完毕?
①结论及理由是:_________________________________________。
②向100毫升18 mol/L的H2SO4溶液中加入足量的铜片并加热,充分反应后,被还原的H2SO4的物质的量
A.小于0·9 mol B.等于0·9 mol C.在0·9 mol与1.8 mol之间 D.大于1·8 mol
③50g的胆矾加热到100℃失去部分结晶水后,质量变为35.6g,则失去水后的硫酸铜晶体的化学式是
A.CuSO4·H2O B.CuSO4·2H2O C.CuSO4·3H2O D.CuSO4
(2)足量的锌投入到一定量的浓硫酸中,充分反应后共收集到SO2和H222.4L(标准状况)。
①简述能产生H2的原因是____________ __________________
②上述变化中体现浓硫酸强氧化性的反应方程式是:
③反应共消耗金属锌的质量为_________g。
④以上数据能否计算出消耗的硫酸的物质的量? _ (填“能”或“不能”)
查看答案和解析>>
科目:高中化学 来源:2015届浙江省高一下学期第一次阶段性测试化学试卷(解析版) 题型:填空题
(1)在试管里放入一小块铜片,注入一定体积的浓硫酸,给试管加热,使之反应。若铜片还有剩余硫酸是否消耗完毕?
①结论及理由是:_________________________________________。
②向100毫升18 mol/L的H2SO4溶液中加入足量的铜片并加热,充分反应后,被还原的H2SO4的物质的量
A.小于0·9 mol B.等于0·9 mol C.在0·9 mol与1.8 mol之间 D.大于1·8 mol
③50g的胆矾加热到100℃失去部分结晶水后,质量变为35.6g,则失去水后的硫酸铜晶体的化学式是
A.CuSO4·H2O B.CuSO4·2H2O C.CuSO4·3H2O D.CuSO4
(2)足量的锌投入到一定量的浓硫酸中,充分反应后共收集到SO2和H222.4L(标准状况)。
①简述能产生H2的原因是____________ __________________
②上述变化中体现浓硫酸强氧化性的反应方程式是:
③反应共消耗金属锌的质量为_________g。
④以上数据能否计算出消耗的硫酸的物质的量? _ (填“能”或“不能”)
查看答案和解析>>
科目:高中化学 来源:同步题 题型:实验题
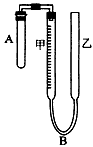
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com