
【题目】某同学欲配制两种一定物质的量浓度的 NaOH溶液。请回答:
(1)①容量瓶上不出现的标识是___(填写字母,下同)
A.容积 B.压强 C.温度 D.密度 E.刻度线
②容量瓶所具备的功能有___。
A.可以长期贮存配制好的溶液 B.可以用来加热溶解固体溶质
C.可以用来作气体发生装置 D.配制一定体积准确浓度的标准溶液
(2)用 NaOH固体配制480mL1mol·L-1NaOH溶液,用托盘天平称取___gNaOH固体。如图为配制过程的某一步操作,该操作名称是___。
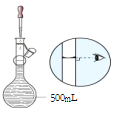
(3)该同学用上述 1mol·L-1NaOH溶液配制 250mL0.1mol·L-1的 NaOH溶液。下列仪器中不必要用到的有___。
①天平 ②烧杯 ③量筒 ④玻璃棒 ⑤容量瓶 ⑥胶头滴管
(4)该同学在两次配制中,以下操作使所配溶液的物质的量浓度偏大的是___。
A.准取称取 NaOH固体,待溶解后立即转移到 100mL容量瓶中并定容
B.定容并摇匀,容量瓶正立后发现液面低于刻度线,继续加蒸馏水定容
C.用少量的 1mol·L-1NaOH溶液洗涤 250mL容量瓶 2~3次
D.向容量瓶中加水至超过刻度线,用胶头滴管吸出后再定容至 100mL。
(5)若向容量瓶中转移溶液时不慎有溶液溅出,处理方法是___。
【答案】BD D 20.0 定容 ① AC 重新配制
【解析】
(1)①容量瓶上的标识有刻度线、温度、容量,不出现的标识是压强和密度。答案为BD
②A.因为若为碱性溶液,会腐蚀容量瓶,所以不能长期贮存配制好的溶液,故错误;
B.容量瓶是不耐热的仪器,所以不能用来加热溶解固体溶质,故错误;
C.容量瓶不耐热,且瓶口小,不易安装带有导管的橡皮塞,所以不能用来作气体发生装置,故错误;
D.配制一定体积准确浓度的标准溶液,正确;
故容量瓶所具备的功能有D。答案为D;
(2)用NaOH固体配制480mL1mol·L-1NaOH溶液,因为没有480mL规格的容量瓶,所以必须选择500mL的容量瓶。
m(NaOH)= 1mol·L-1×0.5L×40g/mol=20.0g。
因为托盘天平的精度低,只能读到小数点后一位,所以称取NaOH固体的质量为20.0g。
如图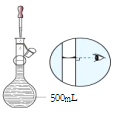 为配制过程中的定容操作。答案为定容;
为配制过程中的定容操作。答案为定容;
(3)该同学用上述 1mol·L-1NaOH溶液配制 250mL0.1mol·L-1的 NaOH溶液。
需计算出V(NaOH)浓= 0.1mol·L-1×0.25L/(1mol·L-1) =0.025L=25.0mL。
用量筒量取,放入烧杯内,加蒸馏水用玻璃棒搅拌溶解,冷却至室温后转移入250mL容量瓶,加水至液面离刻度线1~2cm处,改用胶头滴管加水定容。
故不必要用到的仪器为天平。答案为①;
(4)A.准取称取NaOH固体,待溶解后立即转移到100mL容量瓶中并定容,由于定容后的溶液冷却,导致体积减小,从而使所配溶液浓度偏高;
B.定容并摇匀,容量瓶正立后发现液面低于刻度线,继续加蒸馏水定容,溶液体积偏大,浓度偏小;
C.用少量的 1mol·L-1NaOH溶液洗涤 250mL容量瓶 2~3次,容量瓶内的溶质物质的量偏大,所配溶液的浓度偏高;
D.向容量瓶中加水至超过刻度线,用胶头滴管吸出后再定容至100mL,溶质损失,溶液的浓度偏小。
故使所配溶液的物质的量浓度偏大的操作是AC。答案AC;
(5)若向容量瓶中转移溶液时不慎有溶液溅出,溶质的损失量无法确定,所以需重新配制。
答案为:重新配制。


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
【题目】某学生设计如下实验装置用于制备纯净的Cl2。
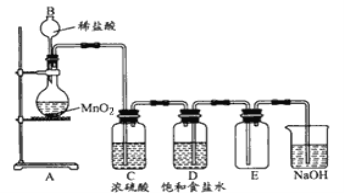
(1)装置中有五处错误,请指出
①_______________
②_______________
③____________________
④_______________________
⑤_______________________
(2)在更正后的装置图中,洗气瓶(净化气体)中的饱和食盐水、浓硫酸、氢氧化钠溶液的作用分别是: ①饱和食盐水的作用:__________②浓硫酸的作用:_________,③氢氧化钠的作用:_____________
(3)将8.7gMnO2与含14.6gHCl的浓盐酸共热制Cl2,甲同学认为可制得7.1gCl2,乙同学认为制得Cl2的质量小于7.1g,你认为_____ (填“甲”或“乙”)同学正确,理由是________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示是由4个碳原子结合成的4种烃(氢原子没有画出)。
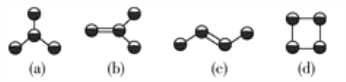
(1)写出有机物(b)的系统命名法的名称:________。
(2)上述有机物中,分子中碳原子一定在同一平面的是______________、______________(填结构简式)。
(3)上述有机物中不能与溴水发生反应使其褪色的有______(填字母代号)。
(4)等质量的上述四种物质完全燃烧耗氧量最大的是______(填结构简式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以孔雀石[主要成分是CuCO3·Cu(OH)2,还含有少量杂质FeO、Fe2O3、SiO2]为原料制备CuSO4·5H2O步骤如下:
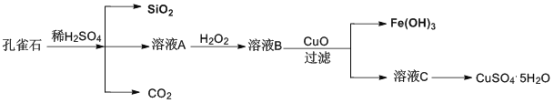
请回答下列问题:
(1)溶液A的金属离子有Fe3+和___。检验溶液A中含有Fe3的试剂是___。
(2)溶液A中加入H2O2的目的是___,发生的离子方程式为___。
(3)由溶液C获得CuSO4·5H2O,需要经过加热蒸发、___、过滤等操作。
(4)溶液B与CuO反应生成Fe(OH)3和溶液C的化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在“绿色化学”工艺中,理想状态是反应中原子全部转化为欲制的产物,即原子利用率为100%。在一定条件下的以下反应中,最符合绿色化学概念的是( )
A. 用水吸收二氧化氮得到硝酸B. 铝盐溶液与氨水反应制氢氧化铝
C. 苯与液溴反应制溴苯D. 乙烯与氯化氢反应制备氯乙烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取表面部分氧化的镁条8.00g溶于250mL4.00mol·L-1的稀盐酸中,向所得溶液中滴加未知浓度的NaOH溶液,产生沉淀的质量与NaOH溶液的体积关系如图所示:
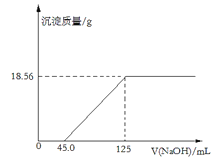
请计算:
(1)NaOH溶液的物质的量浓度___mol·L-1。
(2)样品中镁元素的质量___g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室某浓盐酸试剂瓶上的标签的有关内容,试根据标签上的有关数据回答下列问题:

(1)将标准状况下___L氯化氢气体通入1.00L水中可得36.5%的浓盐酸,该浓盐酸中HCl的物质的量浓度为___mol·L-1。
(2)取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是_____。
A.溶液中HCl的物质的量 B.溶液的浓度 C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.400mol/L的稀盐酸。
①该学生需要量取___mL上述浓盐酸进行配制。
②配制仪器除烧杯、量筒和玻璃棒,还需要的仪器是___、____。
③配制时,下列操作正确的顺序是(用字母表示)____。
A.洗涤 B.定容 C.溶解 D.摇匀 E.冷却 F.称量 G.转移
④在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在括号内填“偏大”、“偏小”或“无影响”)。
Ⅰ.未等稀释后的溶液冷却到室温就转移到容量瓶(______)
Ⅱ.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水。(______)
Ⅲ.配制时,容量瓶有少量蒸馏水(______)
Ⅳ.定容时仰视刻度线。(_______)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)合成高分子化合物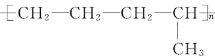 的单体是______;(写结构简式)
的单体是______;(写结构简式)
(2)1mol乳酸( ![]() )最多消耗_______molNa;两分子乳酸在浓硫酸加热的条件下,可生成一种环状酯,写出此酯的结构简式:__________;
)最多消耗_______molNa;两分子乳酸在浓硫酸加热的条件下,可生成一种环状酯,写出此酯的结构简式:__________;
(3)有机物M的结构简式为: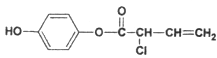 ,则:1 mol M最多消耗的H2、Br2的物质的量比值为_________________;1 mol M最多消耗NaOH的物质的量为______________mol.
,则:1 mol M最多消耗的H2、Br2的物质的量比值为_________________;1 mol M最多消耗NaOH的物质的量为______________mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列不能用勒夏特列原理解释的事实是( )
A.棕红色的NO2加压后颜色先变深后变浅
B.氢气、碘蒸气、碘化氢气体组成的平衡体系加压后颜色变深
C.黄绿色的氯水光照后颜色变浅
D.合成氨工业使用高压以提高氨的产量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com