
| 实验方案 | 实验现象 |
| 1.用砂纸擦后的镁带与热水反应,再向反应后溶液中滴加酚酞 | A.浮于水面,熔成一个小球,在水面上无定向移动,随之消失,溶液变红色 |
| 2.向Na2S溶液中滴加新制的氯水 | B.产生气体,可在空气中燃烧,溶液变成浅红色 |
| 3.钠与滴有酚酞试液的冷水反应 | C.反应不十分强烈,产生的气体可以在空气中燃烧 |
| 4.镁带与2mo1•L-1的盐酸反应 | D.剧烈反应,产生可燃性气体 |
| 5.铝条与2mo1•L-1的盐酸反应 | E.生成白色胶状沉淀,既而沉淀消失 |
| 6.向A1Cl3溶液滴加NaOH溶液至过量 | F.生成淡黄色沉淀 |
| 实验方案 | 实验现象 | 有关化学方程式 |
分析 (1)实验目的为同周期元素性质递变规律;
(2)根据实验步骤来选择所需的实验仪器;
(3)金属的金属性越强,其单质与酸或水反应越剧烈,氢氧化铝能溶于强碱NaOH溶液生成可溶性的偏铝酸钠,硫化钠能被氯气氧化;
(4)元素的金属性越强,金属与水或与酸反应的剧烈程度,其最高价氧化物的水化物的碱性越强;非金属的非金属性越强,其单质的氧化性越强;
(5)同周期由左向右原子半径逐渐减小,核电核数逐渐增大,则原子核对核外电子的吸引能力逐渐增强即失电子能力减弱,得电子能力增强;
(6)元素的非金属性越强,其最高价氧化物的水化物酸性越强,强酸能和弱酸盐反应生成弱酸;
(7)本周期单核离子半径最小的粒子是铝离子.
解答 解:(1)根据题意“某同学做同周期元素性质递变规律实验时”以及所做实验可以判断,本实验的实验目的是:验证第三周期元素从左到右金属性递减、非金属性递增的规律.
故答案为:验证第三周期元素从左到右金属性递减、非金属性递增的规律;
(2)根据每个实验过程可知,这些实验要用到的仪器有:试管、酒精灯、镊子、小刀、玻璃片、胶头滴管等;
故答案为:试管、酒精灯、镊子、小刀、玻璃片、胶头滴管等;
(3)根据元素周期表第三周期元素的排列顺序,可确定实验操作顺序和相关的实验现象等(如下表).
| 实验方案 | 实验现象 | 有关化学方程式 |
| 3 | A | 2Na+2H2O═2NaOH+H2↑ |
| 1 | B | Mg+2H2O═Mg(OH)2+H2↑ |
| 4 | D | Mg+2HCl═MgCl2+H2↑ |
| 5 | C | 2Al+6HCl═2AlCl3+3H2↑ |
| 6 | E | AlCl3+3NaOH═Al(OH)3↓+3NaCl Al(OH)3+NaOH═NaAlO2+2H2O |
| 2 | F | H2S+Cl2═2HCl+S↓ |
点评 本题考查性质实验方案设计,为高频考点,侧重考查学生实验操作、实验观察及实验设计能力,明确实验原理、物质性质及其递变规律是解本题关键,熟练掌握第三周期元素周期律并灵活运用,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑥ | B. | ②④⑤ | C. | ①②⑤ | D. | ②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 和
和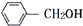 互为同系物,均可以与金属钠反应.
互为同系物,均可以与金属钠反应.| A. | .③④⑤⑥ | B. | ①②③④ | C. | ①②⑤⑥ | D. | ①②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油裂解可以得到氯乙烯 | |
| B. | 油脂水解可得到氨基酸和甘油 | |
| C. | 所有烷烃和蛋白质中都存在碳碳单键 | |
| D. | 蔗糖和麦芽糖的组成都是C12H22O11,水解产物均含有葡萄糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
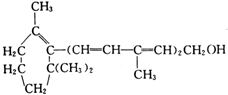
| A. | 1个分子中有5个碳碳双键 | |
| B. | 能使高锰酸钾溶液褪色 | |
| C. | 能与碳酸钠溶液反应放出CO2气体 | |
| D. | 能发生加成反应、氧化反应、置换反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(A)=0.6 mol/(L•min) | B. | v(B)=1.2 mol/(L•min) | ||
| C. | v(C)=1.2 mol/(L•min) | D. | v(B)=0.03 mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| a | b | c | |
| I | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| II | 碱石灰 | 浓硫酸 | 无水氯化钙 |
| III | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com