
| A.S的还原性 | B.S的漂白性 | C.SO2的还原性 | D.SO2的漂白性 |
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源:不详 题型:单选题
| A.无沉淀生成,溶液显红色 | B.无沉淀生成,溶液显无色 |
| C.有沉淀生成,溶液显无色 | D.有沉淀生成,溶液显红色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.相同质量的O2和O3原子个数比为2:3 |
| B.O2和O3化学性质完全相同 |
| C.在相同温度与压强下,等体积的O2和O3含有相同的分子数 |
| D.O2和O3的相互转化是物理变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.大于0.90mol | B.等于0.45mol |
| C.在0.45mol和0.90mol之间 | D.小于0.45mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
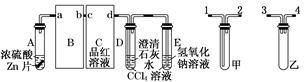
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 o
o

 酸性KMnO4溶液、饱和NaHCO3溶液、品红溶液、澄清石灰水
酸性KMnO4溶液、饱和NaHCO3溶液、品红溶液、澄清石灰水
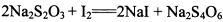 。为测定所制得晶体的纯度,该小组以淀粉作指示剂,用
。为测定所制得晶体的纯度,该小组以淀粉作指示剂,用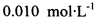 的碘水进行多次取样滴定,测得
的碘水进行多次取样滴定,测得 的含量约为102%。若所用试剂及操作均无不当,产生该结果最可能的原因是______________。
的含量约为102%。若所用试剂及操作均无不当,产生该结果最可能的原因是______________。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
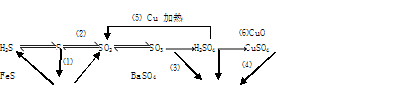
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com