
| A、氯化钠溶液中滴入硝酸银溶液 |
| B、铁片置于硫酸铜溶液中 |
| C、金属钠在氯气中燃烧 |
| D、二氧化碳通入澄清石灰水中 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
A、CH3OH(l)+
| ||
| B、2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1452KJ/mol | ||
C、CH3OH(l)+
| ||
| D、2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-1452KJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
 锌电池用锌作负极的电池生活中随处可见,如锌锰干电池、锌锰碱性电池、锌空电池等.
锌电池用锌作负极的电池生活中随处可见,如锌锰干电池、锌锰碱性电池、锌空电池等.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,边长为28.2cm(内空)的立方体容器内所盛有的N2的分子数目约为NA |
| B、在熔融状态下,l mol NaHSO4完全电离出的阳离子数目为2NA |
| C、7.8 g Na2O2含有的阴离子数目为0.2 NA |
| D、标准状况下,22.4L庚烷完全燃烧生成的CO2分子数目为7NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫酸铝溶液中滴加过量浓氨水:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
| B、乙酸钠溶液显碱性原因:CH3COO-+H2O=CH3COOH+OH- |
| C、氢氧化钠溶液吸收少量SO2气体:SO2+2OH-=SO32-+H2O |
| D、漂白粉放置在空气中变质:ClO-+CO2+H2O=HClO+HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 亚硝酰氯(NOCl)是有机合成中的重要试剂,可由NO与Cl2在通常条件下反应得到(NO2与Cl2反应可得硝酰氯).亚硝酰氯的熔点为-64.5℃,沸点为-5.5℃,并且遇水蒸气分解为氮的氧化物和氯化氢.
亚硝酰氯(NOCl)是有机合成中的重要试剂,可由NO与Cl2在通常条件下反应得到(NO2与Cl2反应可得硝酰氯).亚硝酰氯的熔点为-64.5℃,沸点为-5.5℃,并且遇水蒸气分解为氮的氧化物和氯化氢.查看答案和解析>>
科目:高中化学 来源: 题型:
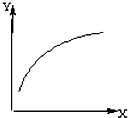 在密闭容器中加入A、B两种物质,在一定条件下反应:2A(s)+B(g)?2C(g) (△H<0).达到平衡后,改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是( )
在密闭容器中加入A、B两种物质,在一定条件下反应:2A(s)+B(g)?2C(g) (△H<0).达到平衡后,改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是( )| X | Y | |
| A | 再加入A | B的转化率 |
| B | 再加入B | C的体积分数 |
| C | 再加入C | B的体积分数 |
| D | 升高温度 | 混合气体密度 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com