
【题目】一种新型电池的工作原理如图所示。该电池工作时,下列说法错误的是
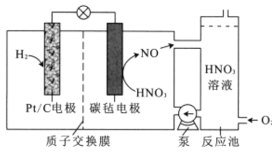
A.Pt/C电极为负极,质子通过交换膜从负极区移向正极区
B.正极的电极反应为NO3-+4H+3e-=NO↑+2H2O
C.反应池中发生总反应4NO+3O2+2H2O=4HNO3,实现HNO3再生
D.理论上,当消耗22.4L(标准状况下)H2时,会消耗1molO2
【答案】D
【解析】
氢气是还原剂,作电池的负极,Pt/C电极为负极,反应为H2-2e-=2H+,质子通过交换膜从负极区移向正极区,硝酸是氧化剂,作电池的正极,正极的电极反应为NO3-+4H+3e-=NO↑+2H2O。
A.氢气是还原剂,作电池的负极,Pt/C电极为负极,反应为H2-2e-=2H+,质子通过交换膜从负极区移向正极区,故A正确;
B.硝酸是氧化剂,作电池的正极,正极的电极反应为NO3-+4H+3e-=NO↑+2H2O,故B正确;
C.从图中可知:NO与O2混合后变成HNO3,进入正极发生电极反应,还原成NO,回到反应池,反应池中发生总反应4NO+3O2+2H2O=4HNO3,实现HNO3再生,故C正确;
D.根据电子守恒,理论上,当消耗22.4L(标准状况下)H2时,会消耗0.5molO2,故D错误;
故选D。


科目:高中化学 来源: 题型:
【题目】下列依据热化学方程式得出的结论正确的是
2C(s) +O2(g) =2CO (g) △H2则△H1<△H2
A.已知2SO2(g)+O2![]() 2SO3(g) 为放热反应,则SO2的能量一定高于SO3的能量
2SO3(g) 为放热反应,则SO2的能量一定高于SO3的能量
B.已知C(石墨,s)==C(金刚石,s)△H>0,则金刚石比石墨稳定
C.已知H+(aq)+OH-(aq)=H2O(1)△H=-57.3kJ/mol,则任何酸碱中和反应的热效应均为57.3 kJ
D.已知2C(s) +2O2(g) =2 CO2(g)△H1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为探究铝片和![]() 溶液反应的实验方案及现象。下列说法错误的是( )
溶液反应的实验方案及现象。下列说法错误的是( )
|
| |
无明显现象 | 铝片表面产生细小气泡 | 出现白色浑浊,产生大量气泡(经检验为 |
A.![]() 溶液显碱性的原因:
溶液显碱性的原因:![]()
B.加热和![]() 逸出对
逸出对![]() 水解平衡移动方向的影响是相反的
水解平衡移动方向的影响是相反的
C.对比实验I、Ⅲ,说明![]() 溶液能破坏铝表面的氧化膜
溶液能破坏铝表面的氧化膜
D.推测出现的白色沉淀可能是氢氧化铝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸亚铁晶体(![]() )常用于晒制蓝图。某研究性学习小组对其进行了系列探究。
)常用于晒制蓝图。某研究性学习小组对其进行了系列探究。
I.纯净的草酸亚铁晶体热分解产物的探究
(1)气体产物成分的探究,小组成员采用如下装置(可重复选用)进行实验:

①E中盛装碱石灰的仪器名称为__________________。
②按照气流从左到右的方向,上述装置的接口顺序为![]() ___________尾气处理装置。
___________尾气处理装置。
③实验前先通入一段时间![]() ,其目的是________________________。
,其目的是________________________。
④实验证明气体产物中含有![]() ,依据的实验现象为_________________________________。
,依据的实验现象为_________________________________。
(2)![]() 受热分解时,固体质量随温度变化的曲线如下图所示,写出加热到400℃时,
受热分解时,固体质量随温度变化的曲线如下图所示,写出加热到400℃时,![]() 晶体受热分解的化学方程式_________________________。
晶体受热分解的化学方程式_________________________。

(3)晒制蓝图时,以![]() 溶液为显色剂,写出
溶液为显色剂,写出![]() 与
与![]() 溶液反应的化学方程式____________。
溶液反应的化学方程式____________。
Ⅱ.草酸亚铁晶体样品纯度的测定
(4)工业制得的草酸亚铁晶体中常含有![]() 杂质测定其纯度的步骤如下:
杂质测定其纯度的步骤如下:
步骤1:称取![]() 草酸亚铁晶体样品溶于稀
草酸亚铁晶体样品溶于稀![]() 中,配成
中,配成![]() 溶液;
溶液;
步骤2:取上述溶液![]() ,用
,用![]() ,标准液滴定至终点消耗标准液
,标准液滴定至终点消耗标准液![]() ;
;
步骤3:向反应后溶液中加入适量锌粉充分反应后加人适量稀![]() ,再用
,再用![]() 标准液滴定至终点,消耗标准液
标准液滴定至终点,消耗标准液![]()
①步骤2中滴定终点的现象为_______________,,步骤3中加入锌粉的目的是__________________。
②草酸亚铁晶体样品的纯度为_________________(写出计算表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】采用下列装置和操作,能达到实验目的的是

A. 用装置甲分离出溴苯 B. 用装置乙验证乙炔的还原性
C. 用装置丙制取乙烯 D. 用装置丁制取乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】他米巴罗汀是一种对白血病、阿尔茨海默症等疾病具有较好治疗效果的药物,其一种合成路线:
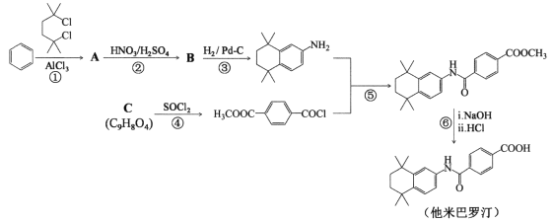
回答下列问题:
(1)A的结构简式是_________,C中含氧官能团的名称是_________
(2)①和③的反应类型分别是_________
(3)下列说法正确的是_________(填标号)。
a.A为苯的同系物b.B的一氯代物有5种
c.1molC最多可与2molNaOH反应d.弱碱性条件有利于反应⑤进行
(4)草酰氯![]() 与乙二胺(
与乙二胺(![]() )反应可得到一种六元环状化合物,该反应的化学方程式为_________
)反应可得到一种六元环状化合物,该反应的化学方程式为_________
(5)化合物W与C互为同分异构体,且满足下列条件:①属于芳香族化合物且能与NaHCO3反应:②能发生银镜反应;③酸性条件下可发生水解反应,其产物能之一与FeCl3发生显色反应,则W共有_________种,其中一种核磁共振氢谱为1:2:2:2:1,其结构简式为__________。
(6)参照上述合成路线,设计由苯和1,3-丁二烯合成![]() 的路线(其它无机试剂任选)。__________
的路线(其它无机试剂任选)。__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以煤为原料可合成涂料H(如下图)。B分子式为C2H6O,能与钠反应放出氢气。(注:流程中某些反应条件没有给出)。
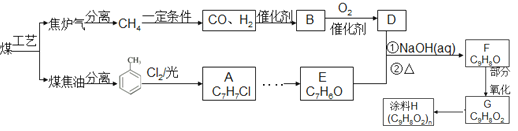
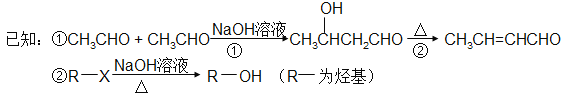
请回答:
(1)流程中煤的综合利用的工艺名称为 。
(2)B的结构简式是 ,E中含氧官能团的名称是 。
(3)G→H反应的化学方程式 。
(4)对于化合物F,下列说法正确的是 。
A、能发生银镜反应 B、能使Br2的CCl4溶液褪色
C、能发生水解反应 D、能与金属钠反应
(5)下列有机物与G不是互为同分异构体的是 。
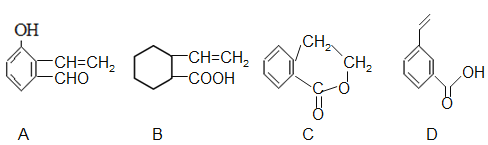
(6)从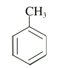 →E 的合成路线(试剂及溶剂任选:合成路线参照“已知①”中书写形式) 。
→E 的合成路线(试剂及溶剂任选:合成路线参照“已知①”中书写形式) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将不同量的CO(g)和H2O(g)分别通入体积为2 L的恒容密闭容器中,进行反应:CO(g) + H2O(g) ![]() CO2(g) + H2(g),得到如下三组数据:
CO2(g) + H2(g),得到如下三组数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | |
CO | H2O | CO2 | |||
1 | 650 | 4 | 2 | 1.6 | 5 |
2 | 900 | 2 | 1 | 0.4 | 3 |
3 | 2 | 1 | 0.4 | 1 | |
下列说法不正确的是
A. 该反应的正反应为放热反应
B. 实验1中,前5min用CO表示的速率为0.16 mol/(L·min)
C. 实验2中,平衡常数K=1/6
D. 实验3跟实验2相比,改变的条件可能是温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.标准状况下,22.4L15NH3中含有的质子数为11NA
B.含63gHNO3的浓硝酸与足量铜完全反应,转移电子数大于0.5NA
C.常温下,1L![]() 溶液中含有的氮原子数小于0.2NA
溶液中含有的氮原子数小于0.2NA
D.标准状况下,224mLSO2溶于水后形成的溶液中![]() 、
、![]() 、
、![]() 粒子数之和等于0.01NA
粒子数之和等于0.01NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com