
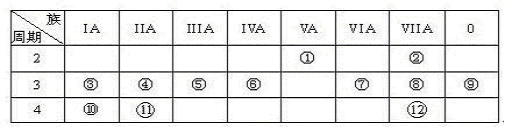
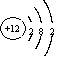 (1分) 、
(1分) 、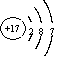 (1分)
(1分)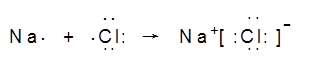 (2分)
(2分)


 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:高中化学 来源:不详 题型:单选题
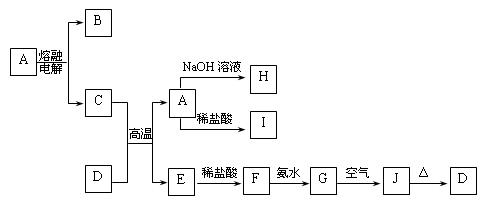
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.同周期的主族元素中,ⅦA族元素的原子半径最小 |
| B.元素周期表中从ⅢB到ⅡB十个纵列的元素都是金属元素 |
| C.室温条件下,O族元素的单质都是气体 |
| D.ⅥA元素的原子,其半径越大,越容易得到电子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.a - c ="" m -n | B.b-d =" m" + n |
C.a>b>d >c >c | D.a>c>b>d |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 元素 | F | Cl | Br | I | ||||
| 氢化物组成 | HF | HCl | HBr | HI | ||||
| 氢化物形成难易程度 | H2、F2混合,冷暗处剧烈化合并发生爆炸 | H2、Cl2混合,光照或点燃时发生爆炸 | H2与Br2混合,加热发生化合 | H2、I2混合,加热化合,同时又分解 | ||||
| 氢化物热稳定性 | 很稳定 | 稳定 | 较稳定 | 较不稳定
查看答案和解析>> 科目:高中化学 来源:不详 题型:单选题 短周期元素A、B、C原子序数依次递增,它们的原子的最外层电子数之和为10。A与C在周期表中同主族,B原子最外层电子数等于A原子次外层电子数。下列叙述正确的是 A.原子半径B>C>A B.氧化物的熔点B>A C.A与C能形成离子化合物 D.氢化物的稳定性C>A 查看答案和解析>> 同步练习册答案 湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区 违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com版权声明:本站所有文章,图片来源于网络,著作权及版权归原作者所有,转载无意侵犯版权,如有侵权,请作者速来函告知,我们将尽快处理,联系qq:3310059649。 ICP备案序号: 沪ICP备07509807号-10 鄂公网安备42018502000812号 |