
| 1 |
| 2 |
| 3 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |
| C4(H2O) |
| C4(H2) |
| C4(H2O) |
| C4(H2) |


科目:高中化学 来源: 题型:
| A、①④ | B、③④ | C、③⑤ | D、②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素D的单质只能做氧化剂 |
| B、元素B和D可以形成化学式为BD3的共价化合物 |
| C、A、B两种元素形成的化合物的空间构型一定是三角锥形 |
| D、元素A、C不可能形成结构式为A-C-C-A的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 7 |
| 2 |
| A、通乙烷的电极为正极 |
| B、参加反应的O2与C2H6的物质的量比为7:2 |
| C、放电一段时间后,KOH的物质的量浓度不变 |
| D、电解质溶液中,CO32-向正极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
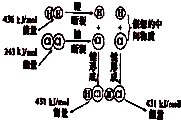 如图所示是101kPa时氢气在氯气中燃烧生成氯化氢气体的能量变化,则下列有关说法中不正确的是( )
如图所示是101kPa时氢气在氯气中燃烧生成氯化氢气体的能量变化,则下列有关说法中不正确的是( )| A、1molH2中的化学键断裂时需要吸收436kJ能量 |
| B、2molHCl分子中的化学键形成时要释放862kJ能量 |
| C、稳定性:H2(g)>HCl(g) |
| D、此反应的热化学方程式为:H2(g)+Cl2(g)=2HCl(g)△H=-248kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com