
实验方案 | 实验现象 |
①用砂纸打磨后的镁带与沸水反应,再向反应液中滴加酚酞试液 | A.浮于水面,溶成小球,在水面上无定向移动,随之消失,溶液变成红色 |
②向新制的饱和Na2S溶液中滴加新制的氯水 | B.有气体产生,溶液变成浅红色 |
③钠与滴有酚酞试液的冷水反应 | C.反应不十分剧烈,有气体产生 |
④镁带与稀盐酸反应 | D.剧烈反应,有气体产生 |
⑤铝条与稀盐酸反应 | E.生成白色胶状沉淀,继而沉淀消失 |
⑥向氯化铝溶液中滴加氢氧化钠溶液至过量 | F.生成淡黄色沉淀 |
请你帮助该同学整理并完成实验报告
(1)实验目的:______________________________________________________。
(2)实验用品:仪器:①____________ ②____________ ③____________
④试管夹 ⑤镊子 ⑥小刀 ⑦玻璃片 ⑧砂纸 ⑨火柴
药品:钠、镁带、铝条、稀盐酸、新制氯水、饱和Na2S溶液、AICl3溶液、氢氧钠溶液、酚酞试液。
(3)实验内容:(填写与实验方案相对应的实验现象和有关化学反应的离子方程式
实验方案 | 实验现象(填写字母) | 离子方程式 |
① |
|
|
② |
|
|
③ |
|
|
④ |
|
|
⑤ |
|
|
⑥ |
|
|
(4)实验结论:___________________________________________________________。
请从原子结构理论方面简单说明具有上述结论的原因_________________________。
(5)请你补充一个实验方案(简单易行),证明此周期中另两种主族元素的性质递变规律。
_____________________________________________________________________。
(1)同周期元素的金属性和非金属性的递变规律
(2)仪器:试管、酒精灯、胶头滴管
(3)
实验方案 | 实验现象 | 有关化学方程式(是离子反应的只写离子方程式) |
① | B |
|
② | F | S2-+Cl2====S↓+2Cl- |
③ | A | 2Na+2H2O====2Na++2OH-+H2↑ |
④ | D | Mg+2H+====Mg2++H2↑ |
⑤ | C | 2Al+6H+====2Al3++3H2↑ |
⑥ | E | Al3++4OH-==== |
(4)实验结论:同周期元素金属性依次减弱;非金属性依次增强 同周期元素原子电子层数相同,从左至右核电荷数逐渐增多,原子半径逐渐减小,原子核对电子的引力逐渐增强,失电子能力逐渐减弱,得电子能力逐渐增强。因此金属性逐渐减弱,非金属性逐渐增强。
(5)方案一:测等浓度的Na2SiO3和Na3PO4溶液的pH,Na2SiO3的pH大,证明H3PO4的酸性强,P的非金属性强。方案二:向Na2SiO3溶液中加H3PO4,产生白色胶状沉淀,证明H3PO4的酸性强,P的非金属性强。(其他合理方案均可)


 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:阅读理解
| 序号 | 实验内容 | 实验现象 |
| A | 取第一份溶液,向其中滴加几滴酚酞试液,反复振荡. | 溶液不变红色 |
| B | 取第二份溶液,先加水稀释,再加少量的二氧化锰,有气泡放出,反复振荡,过滤,向滤液中滴加几滴酚酞试液,反复振荡. | 溶液变红色 |
| C | 取第三份溶液,向其中先加少量的二氧化锰,有气泡放出,反复振荡,过滤,向滤液中滴加几滴酚酞试液,反复振荡. | 溶液也不变红色 |
| D | 取第四份溶液,先加水稀释,再滴加几滴酚酞试液,反复振荡. | 溶液也不变红色 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
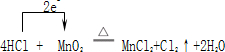
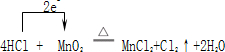
| 实验内容 | 实验现象 | |
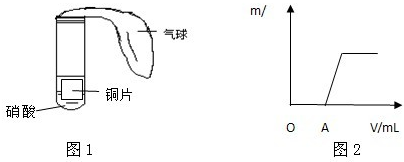
| A | 收集一集气瓶气体,观察颜色,然后向瓶内倒入约占瓶容积1/5的蒸馏水,充分振荡. | 蒸馏水呈浅黄绿色,瓶内气体仍呈黄绿色. |
| B | 取出瓶内部分溶液,滴入紫色石蕊试液中直至过量. | 紫色石蕊试液先变红色,后红色褪色. |
| C | 取出瓶内剩下的部分溶液,滴入硝酸银溶液中. | 产生大量白色沉淀 |
| D | 最后向瓶内倒入少量浓氢氧化钠溶液,振荡. | 瓶内黄绿色气体立即消失. |
查看答案和解析>>
科目:高中化学 来源:江苏模拟题 题型:实验题

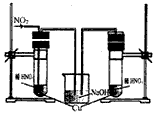
查看答案和解析>>
科目:高中化学 来源: 题型:
请按要求回答下列问题:
(1).某合作学习小组讨论辨析以下说法,其中说法正确的是 _____________
A根据酸分子中含有的氢原子个数,将酸分为一元酸、二元酸等
B 将Na2O2投入FeCl2溶液中, 可观察到的现象是生成红褐色沉淀、有气泡产生
C 金属元素的原子只有还原性,离子只有氧化性
D不锈钢和目前流通的硬币都是合金;
E NH3、CO2的水溶液均能导电,所以NH3、CO2均是电解质
(2)将5mol/L的Mg(NO3)2溶液a mL稀释至b mL,稀释后溶液中NO3-的物质的量浓度为_____________
(3)在K2Cr2O7+14HCl==2KCl+2CrCl3+3Cl2↑+7H2O反应中,
氧化剂是_____ _(填化学式) 当有14.6gHCl被氧化时,电子转移为 mol。
(4)学校研究性学习小组的同学,为测定某含镁3%~5%的铝镁合金(不含其他元素)中镁的质量分数,设计下列实验方案进行探究,填写下列空白:
实验方案:铝镁合金 ![]()
![]() 测定剩余固体质量。
测定剩余固体质量。
① 实验中发生反应的化学方程式是__________________。
② 实验步骤:称取5.4 g铝镁合金粉末样品,投入V mL 2.0 mol/L NaOH 溶液中充分反应。计算所用NaOH溶液的体积V≥______________。
过滤、洗涤、干燥、称量固体。该步骤中若未洗涤固体,测得镁的质量分数将________( 填 不变 偏高 或 偏低 )。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com