
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| 1.5mol |
| 2mol |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��һ������92.2 kJ |
| B��һ��С��92.2 kJ |
| C��һ������92.2 kJ |
| D����ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��A��B��E��D |
| B��A��B��D��E |
| C��D��E��A��B |
| D��D��A��B��E |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ��� | a | b | c | d | e | f |
| ���� | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | NaAlO2 |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

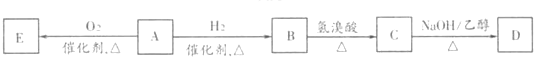
| A���ɲ�ȡ�����������г��ȼ�յķ�������H2S����Ⱦ |
| B����Ӧ���е�������ӦʽΪ2H++2e-�TH2��������������Һ������ |
| C���練Ӧ����H2S��������Ӧ���ӷ���ʽΪ��2Fe3++3H2S�T2FeS��+S��+6H+ |
| D���˷�Ӧ����ͼ�п�ѭ�����õ�������FeCl3��Һ��FeCl3������ɱ�����������;�ˮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� | �۵�/�� | �е�/�� | �ܶ�/��g/cm3�� |
| �Ҵ� | -144 | 78 | 0.789 |
| ���� | 16.6 | 117.9 | 1.05 |
| �������� | -83.6 | 77.5 | 0.90 |
| Ũ���� | -- | 338 | 1.84 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
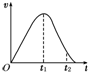 �ѳ�ȥ����Ĥ��þ������ʢ��һ��Ũ�ȵ�ϡ������Թ��У�����H2����������v��ʱ��t�ı仯��ϵ��ͼ��ʾ������O��t1�����ʱ仯����Ҫ������
�ѳ�ȥ����Ĥ��þ������ʢ��һ��Ũ�ȵ�ϡ������Թ��У�����H2����������v��ʱ��t�ı仯��ϵ��ͼ��ʾ������O��t1�����ʱ仯����Ҫ�������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ������������ʣ� | �����Լ� | ���뷽�� | |
| A | �������֣����ᣩ | ����̼������Һ | ���� |
| B | ��֬�����ƣ����ͣ� | NaCl���� | ���� |
| C | �����������Ҵ��� | ����������Һ | ��Һ |
| D | �������ӣ� | Ũ��ˮ | ���� |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com