
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,1mol H2O的体积为22.4L | |
| B. | 1mol•L-1的氯化钠溶液是指此溶液中含有1mol NaCl | |
| C. | 从1L 1mol•L-1的NaCl溶液中取出100mL溶液,其物质的量浓度变为0.1mol•L-1 | |
| D. | 以g•mol-1为单位时,在数值上摩尔质量与相对分子质量或相对原子质量相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 11.2L | B. | 5.6L | C. | 4.48L | D. | 2.24L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu(OH)2和H2SO4;Cu(OH)2和CH3COOH | B. | Ba(OH)2和Na2SO4;Ba(OH)2和CuSO4 | ||
| C. | NaOH和H2SO4;NaOH和NaHSO4 | D. | Na2CO3和盐酸;NaHCO3和盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaAlO2溶液和盐酸 | B. | NaHCO3溶液和Ca(OH)2溶液 | ||
| C. | Ba(OH)2溶液和浓MgCl2溶液 | D. | 稀硫酸和碳酸氢钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 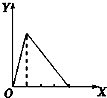 向NaOH溶液中逐滴加入AlCl3溶液至过量且边滴边振荡 | |
| B. | 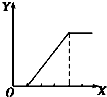 向NaAlO2溶液中滴加稀盐酸至过量且边滴边振荡 | |
| C. | 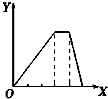 向NH4Al(SO4)2溶液中逐滴加入氢氧化钠溶液直至过量 | |
| D. | 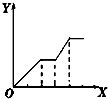 向NaOH、Ba(OH)2、NaA1O2的混合溶液中逐渐通入二氧化碳至过量 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
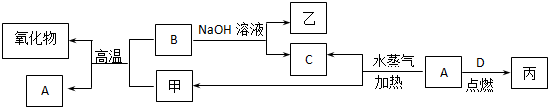
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同浓度、同体积的强酸与强碱溶液混合后,溶液的pH=7 | |
| B. | 在含有BaSO4沉淀的溶液中加入Na2SO4固体,c(Ba2+)增大 | |
| C. | 二氧化碳溶于水能部分电离,故二氧化碳属于弱电解质 | |
| D. | 在CH3COONa溶液中加入适量CH3COOH,可使c(Na+)═c(CH3COO-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com