
在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是
A.甲的分子数比乙的分子数多 B.甲的物质的量比乙的物质的量小
C.气体摩尔体积:甲<乙 D.甲的相对分子质量比乙的相对分子质量小
 综合自测系列答案
综合自测系列答案科目:高中化学 来源:2016-2017学年山西省高一上期中化学试卷(解析版) 题型:选择题
常温下,欲配制密度为1.10 g·cm-3、浓度为6 mol·L-1的稀盐酸,在体积为100 mL、密度为1.19 g·cm-3、浓度为12 mol·L-1的浓盐酸中需加蒸馏水
A.200 mL B.100 mL C.101 mL D.120 mL
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省洛阳市高一上学期期中化学试卷(解析版) 题型:计算题
车用妄全气囊中反应方程式为NaN3=2Na+3N2↑,用双桥线标出电子转移的数目和变化类型,指出氧化剂和还原剂。若要得到标准状况下33.6 LN2,需要多少克NaN3(写出计算过程),NaN3的密度约为2 g/cm3,则NaN3的体积约为多少立方厘米。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市武清区等五区县高一上期中化学试卷(解析版) 题型:填空题
一个体重50kg的健康人体内含铁元素2g,这2g铁元素以Fe2+和Fe3+的形式存在。Fe2+易被吸收,所以给贫血者补充铁时,应补充含Fe2+的亚铁盐(如FeSO4)。服用维生素C可使食物中的Fe3+转化成Fe2+,有利于人体对铁的吸收。请回答下列问题:
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是____________。
A .Fe B.Fe2+ C.Fe3+
(2)维生素C可使食物中的Fe3+转化为Fe2+,在此过程中__________是氧化剂,说明维生素C具有 性。
(3)在人体中进行Fe2+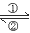 Fe3+的转化时,①反应中的Fe2+发生 反应,②反应中的Fe3+被_______________。
Fe3+的转化时,①反应中的Fe2+发生 反应,②反应中的Fe3+被_______________。
(4)市场上出售的某种麦片中含有微量的颗粒细小的还原性铁粉,这些铁粉在人体胃酸(主要成分是盐酸)的作用下转化成亚铁盐。此反应的化学方程式为___________________________,离子方程式为_________________________。
(5)己知下列反应:
①H2O2+2Fe3+=2Fe2++O2↑+2H+②2Fe2++H2O2+2H+=2Fe3++2H2O
反应①中生成1 molO2转移电子的物质的量为__________,反应①、②的总反应方程式为______________________,
在该反应中Fe3+的作用为________________。
(6)在Fe+4HNO3=Fe(NO3)3+NO↑+2H2O的反应中, HNO3表现了___________性和_____________ 性,毎有1 molFe参加反应转移电子______________mol。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市武清区等五区县高一上期中化学试卷(解析版) 题型:选择题
归纳是学习化学的一种常用方法,某同学归纳的物质及其所属类別与右图的对应关系正确的是
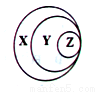
A.X—胶体;Y—混合物;Z—淀粉溶液
B.X—化合物;Y—含氧酸盐;Z—氯化钠
C.X—气态氢化物;Y—酸;Z—盐酸
D.X—强电解质;Y—强酸;Z—硫酸
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市武清区等五区县高一上期中化学试卷(解析版) 题型:选择题
室温下,在强酸性和强碱性溶液中都不能大量共存的离子组是
A. NH4+、Cu2+、 Cl-、NO3- B.K+、Na+、CO32-、S2-
C. K+、Na+、 CH3COO-、SO42- D.Ba2+、Mg2+、HCO3-、Cl-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年新疆生产建设兵团二中高二上期中化学卷(解析版) 题型:选择题
常温下,0.01 mol·L-1 MOH溶液的pH为10,MOH(aq)与H2SO4(aq)反应生成1 mol正盐的ΔH=-24.2 kJ·mol-1,强酸与强碱的稀溶液的中和热为ΔH=-57.3 kJ·mol-1。则MOH在水溶液中电离的ΔH为
A.-69.4 kJ·mol-1 B.-45.2 kJ·mol-1 C.+69.4 kJ·mol-1 D.+45.2 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省六校协作体高一上期中化学试卷(解析版) 题型:实验题
(1)现需要配制450 mL 1 mol·L-1硫酸溶液,需用质量分数为98%、密度为1.84 g·cm-3的浓硫酸__________mL。需用 mL 容量瓶。
(2)从上述仪器中,按实验使用的先后顺序,其编号排列是__________。
(3)定容:继续向容量瓶中加蒸馏水至液面距刻度线1~2 cm,改用__________小心滴加蒸馏水至溶液凹液面底部与刻度线相切。如果不小心加多,应该____________
(4)若实验遇到下列情况,对硫酸溶液的物质的量浓度有何影响(填“偏高”、“偏低”或“不变”)。
①用以稀释硫酸的烧杯未洗涤,____________。
②未经冷却趁热将溶液注入容量瓶中,____________。
③定容时观察液面俯视,____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com