
【题目】二氧化碳的有效回收利用,既能够缓解能源危机,又可减少温室效应的影响,具有解决能源问题及环保问题的双重意义。请回答下列问题:
(1)CO2的电子式为___________。
(2)Zn/ZnO热化学循环还原CO2制CO的原理如下图:
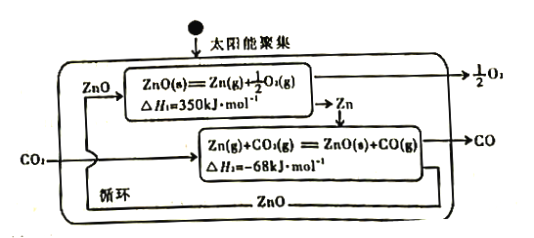
①从循环结果看,能量转化的主要方式是_________________________________。
②反应2CO2(g)=2 CO(g) +O2(g) △H=___________kJ·mol-1。
(3)二甲醚是重要的有机中间体,在一定条件下利用CO2与H2可直接合成二甲醚:
2CO2(g)+6H2(B)![]() CH3OCH3(g)+3H2O(g),当n(H2)/n(CO2)=3时,实验测得CO2的平衡转化率随温度及压强变化如下图所示。
CH3OCH3(g)+3H2O(g),当n(H2)/n(CO2)=3时,实验测得CO2的平衡转化率随温度及压强变化如下图所示。
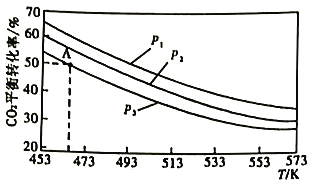
①该反应的△H___________0(填“>”或“<")。
②上图中的压强(p)由大到小的顺序为___________。
③若在1L密闭容器中充入0.2molCO2和0.6molH2,CO2的平衡转化率对应上图中的A点,则在此温度下,该反应的化学平衡常数为___________(保留整数)。
④合成二甲醚过程中往往会生成一氧化碳,合成时选用硅铝混合物作催化剂,硅铝比例不同,生成二甲醚或一氧化碳的物质的量分数不同。硅铝比与产物选择性如下图所示。
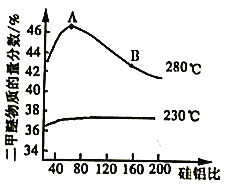
图中A点和B点的化学平衡常数比较:KA___________KB(填“>、=、<")。根据以上两条曲线,写出其中一条变化规律:____________________________________________。
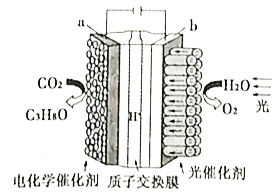
(4)利用电化学原理将H2O和CO2转化为O2和燃料(C3H8O)的实验装置如下图所示。a电极的电极反应式为_________________________________。
 .
.
【答案】![]() 太阳能转化为化学能 564 < p1>p2>p3 23 = a.温度越高,二甲醚的选择性(或物质的量分数)越大;b.低温时硅铝比对二甲醚的选择性(或物质的量分数)影响不大,高温时随着硅铝比增大,二甲醚的选择性(或物质的量分数)先增大后减小。 3CO2+18H++18e-=C3H8O+5H2O
太阳能转化为化学能 564 < p1>p2>p3 23 = a.温度越高,二甲醚的选择性(或物质的量分数)越大;b.低温时硅铝比对二甲醚的选择性(或物质的量分数)影响不大,高温时随着硅铝比增大,二甲醚的选择性(或物质的量分数)先增大后减小。 3CO2+18H++18e-=C3H8O+5H2O
【解析】
(1)可以根据价键规则书写CO2的电子式,注意检查是否满足8电子稳定结构;
(2)仔细分析图像可知在太阳能的作用下实现了反应2CO2(g)= 2CO(g)+O2(g),再利用盖斯定律进行计算;
(3)①依据图像,随温度升高,CO的转化率降低确定反应为放热反应;
②2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g)正反应为气体分子数减小的反应,温度一定时,压强越大,CO2的转化率越大;
CH3OCH3(g)+3H2O(g)正反应为气体分子数减小的反应,温度一定时,压强越大,CO2的转化率越大;
③根据A点,利用三段式法计算平衡常数;
④平衡常数只受温度影响,图中280℃下的A点和B点的平衡常数相等;从图中两条曲线的变化趋势及对比情况可以看出:230℃的曲线变化相对平缓,280℃的曲线变化程度较大且先升后降,280℃二甲醚物质的量分数较大,温度升高,二甲醚的物质的量浓度的变化受影响的程度也有所改变;
(4)a与电源负极相连,所以a是阴极,CO2发生还原反应生成C3H8O,据此书写电极反应式。
(1)根据价键规则,CO2的电子式为![]() ;
;
正确答案:![]() 。
。
(2)仔细分析图像可知在太阳能的作用下实现了反应2CO2(g)= 2 CO(g) +O2(g),所以实现了太阳能向化学能转化;利用盖斯定律进行计算将已知两个热化学方程式相加后再乘以2即得2CO2(g)= 2 CO(g) +O2(g) △H=564kJ/mol;
正确答案:太阳能转化为化学能 564。
(3) ①依据图像,随温度升高,CO的转化率降低,确定反应为放热反应,ΔH<0;
正确答案:<。
②2CO2(g)+6H2(B)![]() CH3OCH3(g)+3H2O(g)正反应为气体分子数减小的反应,温度一定时,压强越大,CO2的转化率越大,根据图像温度相同时CO2的转化率:p1>p2>p3,则图中压强由大到小的顺序为p1>p2>p3;
CH3OCH3(g)+3H2O(g)正反应为气体分子数减小的反应,温度一定时,压强越大,CO2的转化率越大,根据图像温度相同时CO2的转化率:p1>p2>p3,则图中压强由大到小的顺序为p1>p2>p3;
正确答案:p1>p2>p3。
③根据A点,利用三段式法计算平衡常数;
2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g)
CH3OCH3(g)+3H2O(g)
起始量(mol/L)0.2 0.6 0 0
反应量(mol/L)0.1 0.3 0.05 0.15
平衡梁(mol/L)0.1 0.3 0.05 0.15
K=![]() ≈23;
≈23;
正确答案:23。
④平衡常数只受温度影响,图中280℃下的A点和B点的平衡常数相等;从图中两条曲线的变化趋势及对比情况可以看出:230℃的曲线变化相对平缓,280℃的曲线变化程度较大且先升后降,280℃二甲醚物质的量分数较大,温度升高,二甲醚的物质的量浓度的变化受影响的程度也有所改变等,故可以概括为:a.温度越高,二甲醚的选择性越大;b.低温时硅铝比对二甲醚的选择性影响不大,高温时随着硅铝比增大,二甲醚的选择性先增大后减小;
正确答案:a.温度越高,二甲醚的选择性(或物质的量分数)越大;b.低温时硅铝比对二甲醚的选择性(或物质的量分数)影响不大,高温时随着硅铝比增大,二甲醚的选择性(或物质的量分数)先增大后减小。
(4)a与电源负极相连,所以a是阴极,CO2发生还原反应生成C3H8O,电极反应式为3CO2+18H++18e-=C3H8O+5H2O;
正确答案:3CO2+18H++18e-=C3H8O+5H2O。


 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】如图为实验室制取纯净、干燥的氯气,并验证氯气性质的装置。其中E瓶放有干燥红色布条;F中为红色的铜网,其右端出气管口放有脱脂棉。

(1)装置C中盛装的溶液是____________,D中试剂的作用是________。
(2)E中的红色布条是否退色?____,写出F中反应的化学反应方程式:____,其反应现象为_____________。
(3)新制氯水呈黄绿色说明其中含有_____,(填化学式,下同),将紫色石蕊溶液滴入可观察到的现象是_________________,说明其中含有__________。
(4)H中的试剂为___________,用来吸收多余氯气。工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白精,该反应的化学方程式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在呼吸面具和潜水艇中可用过氧化钠作为供氧剂。请选用适当的化学试剂和实验用品,用下图中的实验装置进行实验,证明过氧化钠可用做供氧剂。
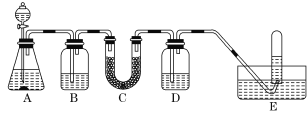
(1)A是制取CO2的装置。写出A中发生反应的化学方程式:______。
(2)填写表中空格:
仪器 | 加入试剂 | 加入该试剂的目的 |
B | 饱和NaHCO3溶液 | 除去CO2中混有的HCl |
C | Na2O2 | _______ |
D | NaOH溶液 | _______ |
(3)写出Na2O2与CO2反应的化学方程式:______。
(4)试管中收集满气体后,下一步实验操作及现象、结论是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一化学兴趣小组在家中进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2接好线路发现灯泡亮,由此得出的结论正确的是

A. NaCl是非电解质
B. NaCl溶液是电解质
C. NaCl在水溶液中电离出了可以自由移动的离子
D. NaCl溶液中产生了电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下图装置进行实验,开始时,a、b两处液面相平,密封好,放置一段时间。下列说法不正确的是( )

A. a管发生吸氧腐蚀,b管发生析氢腐蚀
B. 一段时间后,a管液面高于b管液面
C. a处溶液的pH增大,b处溶液的pH减小
D. a、b两处具有相同的电极反应式:Fe-2e-===Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、D、E均为化学中的常见物质,它们之间的转化关系如图所示(部分产物略去),则下列有关物质的推断不正确的是( )

A. 若A是铁,则E可能为稀硝酸
B. 若A是CuO,E是碳,则B为CO
C. 若A是NaOH溶液,E是CO2,则B为NaHCO3
D. 若A是AlCl3溶液,E可能是氨水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在浓度都为1 mol·L-1的(NH4)2SO4、NH4H CO3、NH4HSO4、NH4Cl的四种溶液中,测得c(NH4+)分别为a、b、c、d(单位为mol·L-1)。下列判断正确的是
A. a=2b=2c=2d B. a>b>c> d C. a>c>d>b D. a>c>b>d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示的是物质A—H相互间的关系(“→”表示物质间的转化关系,“——”表示两端的物质能发生化学反应)。A、G都是常见单质,气体C常用于灭火,D是纯碱,E是熟石灰,F是一种蓝色溶液,可用于配制农药波尔多液。请你回答:
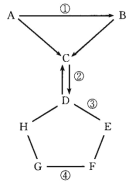
(1)C的化学式__________,H可能是 __________。
(2)写出标号①、②、③、④的化学方程式:
①_____________;②___________ ;
③______________;④__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组模拟工业上从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3等杂质)中提取氧化铝的工艺做实验,流程如下:

请回答下列问题:
(1)操作Ⅰ的名称为_______。
(2)验证溶液B中是否含有Fe3+的方法:_______________________,
(3)不溶物A是___(填化学式),写出D→E反应的离子方程式______________。
(4)说出溶液F中含碳元素溶质的一种用途____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com