
已知:4NH3(g)+5O2(g) == 4NO(g)+6H2O(g) △H="-1" 025kJ/mol,该反应是一个可逆反应。若反应物 起始物质的量相同,下列关于该反应的示意图不正确的是( )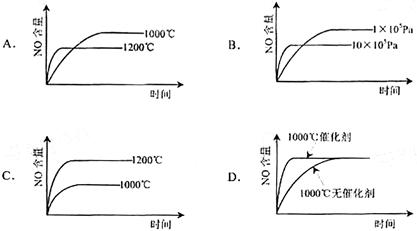
C
解析试题分析:由于该反应的正反应是气体体积增大的放热反应。A.升高温度,化学反应速率加快,达到平衡所需要的时间缩短。当反应达到平衡后,升高温度,根据平衡移动原理,化学平衡向吸热反应方向即向逆反应方向移动,所以NO的平衡含量减小。正确。B.增大压强,物质的浓度增大,反应速率加快,达到平衡所需要的时间缩短。当反应达到平衡后,增大压强,根据平衡移动原理,化学平衡向气体体积减小的方向即向逆反应方向移动,所以NO的平衡含量减小。正确。C.升高温度,平衡向吸热反应方向即向逆反应方向移动,所以NO的平衡含量减小。错误。D加入催化剂后化学反应速率大大加快,达到平衡所需要的时间缩短。当反应达到平衡后,由于催化剂能同等倍数的改变化学反应速率。所以加入催化剂不能使化学平衡发生移动。平衡时NO的含量不变。正确。
考点:考查外界条件对化学反应速率、化学平衡移动影响的知识。


 步步高达标卷系列答案
步步高达标卷系列答案科目:高中化学 来源: 题型:单选题
将BaO2放入密闭的真空容器中,反应2BaO2(s) 2BaO(s)+O2(g)达到平衡。保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是
2BaO(s)+O2(g)达到平衡。保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是
| A.平衡常数减小 | B.BaO量不变 | C.氧气压强不变 | D.BaO2量增加 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
实验室中配制碘水,往往是将I2溶于KI溶液中,即可得到浓度较大的碘水,原因是发生了反应:I2(aq)+I-(aq)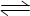 I3-(aq)。在反应的平衡体系中,c(I3-)与温度T的关系如图所示(曲线上的任何一点都表示平衡状态)。
I3-(aq)。在反应的平衡体系中,c(I3-)与温度T的关系如图所示(曲线上的任何一点都表示平衡状态)。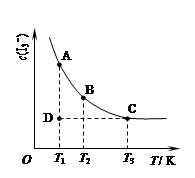
下列说法正确的是
A.该反应的正反应为放热反应
B.A状态与C状态的化学反应速率大小为v(A)>v(C)
C.D状态时,v正>v逆
D.欲配制浓度较大的氯水,可将氯气通入氯化钾溶液中
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
反应4A(g)+5B(g)="=" 4C(g)+ 6D(g)在某密闭容器中进行,半分钟后,C的物质的量浓度增加了0.3mol/L。下列论述正确的是( )
A.半分钟内的平均反应速率:5v(B)=6v(D) B.C的平均反应速率是0.010 mol·L-1·s-1
C.容器中含D的物质的量至少为0.45mol D.容器中A的物质的量浓度增加了0.3mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
mA(g)+nB(g) 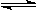 pC(g)+qQ(g)当m、n、p、q为任意整数时,达到平衡的标志是( )
pC(g)+qQ(g)当m、n、p、q为任意整数时,达到平衡的标志是( )
①体系的压强不再改变 ②绝热体系的温度不再改变 ③各组分的浓度不再改变
④各组分的质量分数不再改变 ⑤反应速率vA: vB: vC: vD = m:n:p:q
⑥单位时间内m mol A断键反应,同时p mol C也断键反应
| A.③④⑤⑥ | B.②③④⑥ | C.①③④⑤ | D.①③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
mA(g)+nB(g) 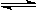 pC(g)+qQ(g)当m、n、p、q为任意整数时,达到平衡的标志是( )
pC(g)+qQ(g)当m、n、p、q为任意整数时,达到平衡的标志是( )
①体系的压强不再改变 ②绝热体系的温度不再改变 ③各组分的浓度不再改变
④各组分的质量分数不再改变 ⑤反应速率vA: vB: vC: vD = m:n:p:q
⑥单位时间内m mol A断键反应,同时p mol C也断键反应
| A.③④⑤⑥ | B.②③④⑥ | C.①③④⑤ | D.①③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知反应2H2(g)+CO(g)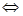 CH3OH(g)的平衡常数如下表。按照相同的物质的量投料,
CH3OH(g)的平衡常数如下表。按照相同的物质的量投料,
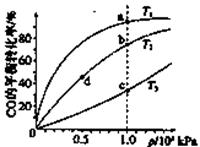
测得CO在不同温度下的平衡转化率与压强的关系如下图所示。下列大小比较正确的是
| 平衡常数 | 温度/℃ | ||
| 500 | 700 | 800 | |
| K | 2.50 | 0.34 | 0.15 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
t ℃时,在体积不变的密闭容器中发生反应:X(g)+3Y(g)  2Z(g),各组分在不同时刻的浓度如下表:
2Z(g),各组分在不同时刻的浓度如下表:
| 物质 | X | Y | Z |
| 初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
| 2 min末浓度/mol·L-1 | 0.08 | a | b |
| 平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com