
| һ������ |
| n(NH3) |
| n(CO2) |
| A���÷�Ӧ��60minʱ�ﵽƽ��״̬ |
| B��NH3��ƽ��ת����Ϊ30% |
| C�����Ӱ�̼�ȿɽ�һ�����CO2��ƽ��ת���� |
| D��A����淴Ӧ���ʦ�����CO2������B�������Ӧ���ʦ�����CO2�� |

| һ������ |
| 1.2 |
| 4 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��H2��I2��HI��Ũ����� |
| B��H2��I2��HI��Ũ�ȱ��ֲ��� |
| C�����������ܶȱ��ֲ��� |
| D�����������������ٸı� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
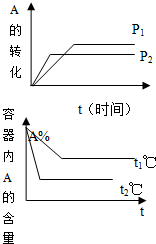
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
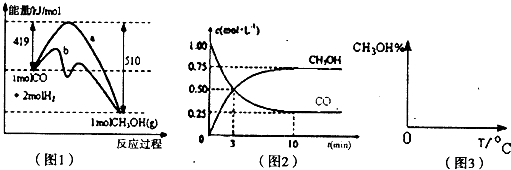
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
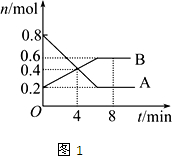
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
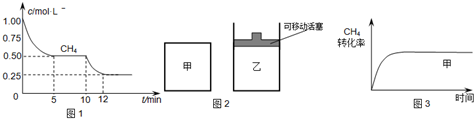
| CO | H2O | CO2 | H2 |
| 0.5mol | 8.5mol | 2.0mol | 2.0mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
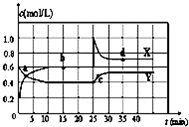
| A��ͼ�е��������ߣ�X�DZ�ʾNO2Ũ����ʱ��ı仯���� |
| B��ǰ10min����v��N2O4����ʾ�Ļ�ѧ��Ӧ����Ϊ0.2mol/��L?min�� |
| C��25minʱ��NO2ת��ΪN2O4�ķ�Ӧ����������ԭ���ǽ��ܱ������������СΪ1L |
| D��ǰ10min����v��NO2����ʾ�Ļ�ѧ��Ӧ����Ϊ0.04mol/��L?min�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ��ʴ���
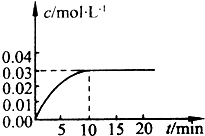
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| һ������ |
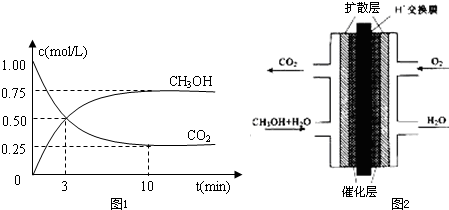
| n(CH3OH) |
| n(CO2) |
| 1 |
| 2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com