
| A. | 白磷晶体中,分子之间通过共价键结合 | |
| B. | 金刚石的网状结构中,由共价键形成的最小碳环上有6个碳原子 | |
| C. | 在NaCl晶体中每个Na+(或Cl-)周围都紧邻6个Cl-或(Na+) | |
| D. | 离子晶体在熔化时,离子键被破坏,而分子晶体熔化时,化学键不被破坏 |
分析 A.白磷为分子晶体;
B.根据金刚石的结构模型 判断;
判断;
C.氯化钠晶体中钠离子或氯离子的配位数都是6;
D.离子晶体的构成微粒是阴阳离子,分子晶体的构成微粒是分子.
解答 解:A.白磷为分子晶体,微粒之间存在分子间作用力,故A错误;
B.金刚石的结构为 ,由模型可知最小的环为六元环,故B正确;
,由模型可知最小的环为六元环,故B正确;
C.氯化钠晶体中钠离子或氯离子的配位数都是6,所以在NaCl晶体中每个Na+(或C1-)周围都紧邻6个Cl-(或Na+),故C正确;
D.离子晶体的构成微粒是阴阳离子,分子晶体的构成微粒是分子,所以离子晶体在熔融状态下能电离出阴阳离子,而分子晶体在熔融状态下还是以分子存在,只破坏分子间作用力不破坏化学键,故D正确;
故选A.
点评 本题考查较为综合,涉及晶体的结构、共价键、氢键等知识,为高频考点,侧重于学生的分析能力的考查,注意相关基础知识的积累,难度不大.


 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:选择题
| A. | v正(CO)=v逆(H2O) | |
| B. | 2 mol H-O键断裂的同时有1 mol H-H键形成 | |
| C. | 生成n mol CO的同时生成n mol H2O(g) | |
| D. | 体系的压强不再发生变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,11.2LCH4中含有的氢原子数为2NA | |
| B. | 1mol氯气跟足量的NaOH溶液完全反应,转移的电子数为2NA | |
| C. | 1mol Na2O含离子数为3NA | |
| D. | 0.1mol/L MgCl2溶液中含氯离子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
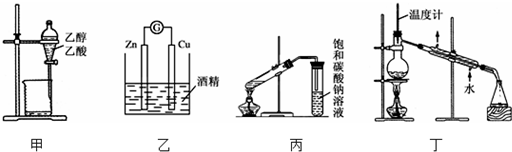
| A. | 甲装置可用来分离乙醇和乙酸 | |
| B. | 乙装置可以构成原电池 | |
| C. | 在制备乙酸乙酯的实验中,丙装置中的饱和碳酸钠可以用氢氧化钠溶液代替 | |
| D. | 丁装置可以用来分离乙醇和丁醇和混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.下列说法正确的是( )
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.下列说法正确的是( )| A. | 正四面体烷的分子式为C4H4,其二氯代物有两种 | |
| B. | 苯为平面六边形结构,分子中存在C-C和C═C,能使酸性KMnO4溶液褪色 | |
| C. | 等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量相同 | |
| D. | 环辛四烯跟苯的结构很像,不能使溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质的量就是物质的质量 | |
| B. | 阿伏加德罗常数就是6.02×1023 | |
| C. | 1mol某物质溶于水一定得阿伏加德罗常数个溶质分子 | |
| D. | 98gH2SO4的物质的量与98gH3PO4的物质的量相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C8H8 | B. | C10H16 | C. | C14H22 | D. | C12H22 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com