
| A. | 制取蒸馏水时,为防止烧瓶内产生暴沸现象,应先向烧瓶中加入几片碎瓷片 | |
| B. | 在气体的制备实验中,若尾气污染空气,一定要用水吸收尾气 | |
| C. | 用加热KMnO4的方法制得的氧气中常带有紫色,实验中应在试管口处放一团棉花 | |
| D. | 在点燃甲烷气体前,为防止爆炸,应先验纯 |
分析 A.加入碎瓷片可以防止暴沸;
B.尾气处理不一定用水吸收;
C.在试管口处放一团棉花可防止高锰酸钾进入水槽;
D.点燃可燃气体应避免爆炸.
解答 解:A.在制取蒸馏水的实验操作中,加入碎瓷片可以防止暴沸,发生危险,故A正确;
B.制取气体时,若是气体有毒,能够污染大气,必须对尾气进行吸收处理,不能直接排放,但是不一定用水吸收,故B错误;
C.加热时试管口放一团棉花的目的是为了防止加热时高锰酸钾粉末进入导管,故C正确;
D.不纯可燃气体在点燃时易爆炸,应先验纯,以避免爆炸,故D正确.
故选B.
点评 本题考查化学实验基本操作,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握实验的安全性以及操作的方法,题目有利于培养学生良好的科学素养,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 化学反应都伴随着热量的变化 | |
| B. | 个别化学反应与能量变化无关 | |
| C. | 某些吸热反应在不加热条件下也能发生 | |
| D. | 放热反应的发生无需任何条件 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
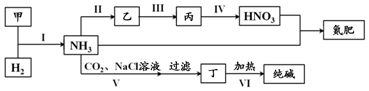
| A. | 甲、乙、丙三种物质中都含有氮元素 | |
| B. | 反应II、III和Ⅳ的氧化剂相同 | |
| C. | VI的产物可在上述流程中被再次利用 | |
| D. | V中发生反应:NH3+CO2+H2O+NaCl═NaHCO3↓+NH4Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知CaO+H2O═Ca(OH)2放出大量的热,故可把该反应设计成原电池 | |
| B. | 因为铁的活泼性强于铜,所以将铁、铜用导线连接后放入浓硝酸中,若能组成原电池,必是铁做负极、铜做正极 | |
| C. | 理论上说,任何能自发进行的氧化还原反应都可设计成原电池 | |
| D. | 某原电池反应为Cu+2AgNO3═Cu(NO3)2+2Ag,装置中的盐桥内可以是含琼脂的KCl饱和溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化铜与硫酸溶液反应:Cu2++2H+═Cu2++H2O | |
| B. | 碳酸钠溶液与盐酸反应:Na2CO3+2H+═2Na++H2O+CO2↑ | |
| C. | 少量CO2通入澄清石灰水中:CO2+Ca2++2OH-═CaCO3↓+H2O | |
| D. | 钠投入到水中:Na+H2O═Na++OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H<0且△S>0的反应肯定是不自发的 | B. | △H<0且△S<0的反应肯定是自发的 | ||
| C. | △H>0且△S>0的反应肯定是自发的 | D. | △H<0且△S>0的反应肯定是自发的 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
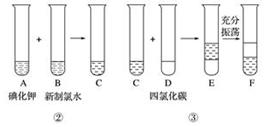
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com