
13C-NMR(核磁共振)、15N-NMR可用于测定蛋白质、核酸等生物大分子的空问结构,Kurt Wu thrich等人为此获得2002年诺贝尔化学奖。下而有关13C、15N叙述正确的是
A.13C与15N有相同的中子数
B.13C与C60互为同素异形体
C.15N与14N互为向位素
D.15N的核外电子数与中子数相同
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源:2015-2016学年河北省邯郸市高一上第一次月考化学试卷(解析版) 题型:选择题
下列实验操作中错误的是
A.蒸发操作时,不能使混合物中的水分完全蒸干后才停止加热
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.过滤操作时,向过滤器中倾倒液体时一定要用玻璃棒引流
D.由于碘在酒精中的溶解度大,所以可用酒精把碘水中的碘萃取出来
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期二调化学试卷(解析版) 题型:实验题
(13分)I.高锰酸钾在实验室和工农业生产中有广泛的用途,实验室以二氧化锰为主要原料制
备高锰酸钾,其部分流程如下:

(1)第①步加热熔融应在铁坩埚中进行,而不用瓷坩埚的原因是 (用化学程式表示)。
(2)第④步通人适量CO2,发生反应生成Mn04和Mn02和碳酸盐,则发生反应的离子方程式为___ _。
(3)第⑥步加热浓缩至液面有细小晶体析出时,停止加热,冷却结晶、过滤、洗涤、干燥,干燥过程中,温度不宜过高,其原因是 (用化学方程式表示)。
(4)H2O2和KMn04都是常用的强氧化剂,若向H2O2溶液中滴加酸性高锰酸钾溶液,则酸性高锰酸钾溶液会褪色,写出该反应的离子方程式:_____ 。
Ⅱ.某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究S02和Cl2的性质。

(5)若从左端分别通人SO2和Cl2,装置A中观察到的现象是否相同? (填“相同”或“不相同”);
(6)若装置B中装有5.0 mL l.0 mol/L的碘水,当通入足量Cl2完全反应后,共转移了5.0×10-2 mol电子,该反应的化学方程式为 。
(7)若由元素S和O组成-2价酸根离子X,X中S和O的质量比为4:3;当Cl2与含X的溶液完全反应后,有浅黄色沉淀产生,取上层清液加入氯化钡溶液,有白色沉淀产生。写出Cl2与含X的溶液反应的离子方程式__ __。
查看答案和解析>>
科目:高中化学 来源:2016届安徽省合肥市高三上第二次段考化学试卷(解析版) 题型:选择题
如图是草酸溶液中 三种微粒的分布分数(某微粒物质的量浓度与三种微粒物质的量浓度和的比值)与pH的关系,下到有关说法不正确的是
三种微粒的分布分数(某微粒物质的量浓度与三种微粒物质的量浓度和的比值)与pH的关系,下到有关说法不正确的是

A.pH=5的溶液中: 
B. 溶液中:
溶液中:

C.向  溶液中加强酸至pH与a点对应时,溶液中
溶液中加强酸至pH与a点对应时,溶液中 
D.为使溶液中c( 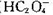 )尽可能多一些,溶液的pH最好控制在2.7左右
)尽可能多一些,溶液的pH最好控制在2.7左右
查看答案和解析>>
科目:高中化学 来源:2015-2016学年西藏日喀则一中高二10月月考化学试卷(解析版) 题型:填空题
(7分)有A、B、C、D、E、F六种元素。已知:
①它们位于三个不同的短周期,核电荷数依次增大。
②B与F同主族。
③B、C分别都能与D按原子个数比1∶1或1∶2形成化合物。
④A、E分别都能与D按原子个数比1∶1或2∶1形成化合物。
⑤E元素的电离能数据如下 (kJ·mol-1):
I1 | I2 | I3 | I4 | … |
496 | 4562 | 6912 | 9540 | … |
(1)写出只含有A、B、D、E四种元素的两种无水盐的化学式________、________。
(2)B2A4分子中存在______个σ键,______个π键。
(3)人们通常把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以用于计算化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。下表列出了上述部分元素形成的化学键的键能:
化学键 | A—A | C—C | A—C |
键能/kJ·mol-1 | 436 | 946 | 390.8 |
试计算A单质与C单质反应生成CA3时的反应热ΔH=_____ (要写单位)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年西藏日喀则一中高二10月月考化学试卷(解析版) 题型:选择题
下列关于主族元素电了排布特征的说法正确的是
A.主族元素的原子核外电子最后填入的能级是s能级
B.主族元素的原子核外电子最后填入的能级是s能级或p能级
C.主族元素的原子核外电子最后填入的能级是d能级或f能级
D.主族元素的原子核外电子最后填入的能级是s能级或d能级
查看答案和解析>>
科目:高中化学 来源:2016届河南省高三第四次大考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.HClO2 →ClO2+Cl2+H2O(未配平), 1 mol HClO2分解时转移电子的物质的量为1 mol
B.标准状况下,14 g CO、C2H4混合气体与11.2 L N2所含有的分子数都是0.5NA
C.与金属Cu常温下反应放出气体的溶液可以存在的离子有:Fe2+、Al3+、SO42-、K+
D.在燃煤时加入适量石灰石,可减少SO2的排放,其中发生的反应为2CaCO3 +O2+2SO2 2CaSO3 +2CO2
2CaSO3 +2CO2
查看答案和解析>>
科目:高中化学 来源:2016届河北省衡水市高三复习班上月考化学试卷(解析版) 题型:选择题
原子序数依次增大的元素a、b、c、d,它们的最外层电子数分别为1、6、7、1。a—的电子层结构与氦相同,b和c的次外层有8个电子,c—和d+的电子层结构相同。下列叙述错误的是
A.元素的非金属性次序为c>b>a
B.a和其他3种元素均能形成共价化合物
C.d和其他3种元素均能形成离子化合物
D.元素a、b、c各自最高和最低化合价的代数和分别为0、4、6
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省五校协作体高三上学期期初考试化学试卷(解析版) 题型:选择题
镍氢电池(NiMH)目前已经成为混合动力汽车的一种主要电池类型。NiMH中的M表示储氢金属或合金。该电池在充电过程中的总反应方程式是:
Ni(OH)2 + M = NiOOH + MH
已知:6NiOOH + NH3 + H2O + OH-=6 Ni(OH)2 + NO2-
下列说法正确的是
A.充电过程中OH-离子从阳极向阴极迁移
B.充电过程中阴极的电极反应式:H2O + M + e-=MH + OH-,H2O中的H被M还原
C.电池放电过程中,正极电极反应式为:NiOOH + H2O + e-= Ni(OH)2 + OH-
D.NiMH电池中可以用KOH溶液、氨水等作为电解质溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com