
【题目】随着石油资源的日趋紧张,天然气资源的开发利用受到越来越多的关注。以天然气(主要成分是CH4)为原料经合成气(主要成分为CO、H2)制化学品,是目前天然气转化利用的主要技术路线。而采用渣油、煤、焦炭为原料制合成气,常因含羰基铁[Fe(CO)5]等而导致以合成气为原料合成甲醇和合成氨等生产过程中的催化剂产生中毒。请回答下列问题:
(1)[Fe(CO)5]中铁的化合价为0,写出铁原子的基态电子排布式:______________________。
(2)与CO互为等电子体的分子为________(填化学式),CO分子的电子式为________。
(3)在CH4、CO、CH3OH中,碳原子采取sp3杂化的分子有________________(填化学式),CH3OH的熔、沸点比CH4高,其主要原因是_________________________________。
【答案】 1s22s22p63s23p63d64s2或[Ar]3d64s2 N2 ![]() CH4、CH3OH CH3OH分子之间有极性,同时分子之间还存在着氢键的作用
CH4、CH3OH CH3OH分子之间有极性,同时分子之间还存在着氢键的作用
【解析】(1)Fe的原子序数为26,则基态电子排布式为[Ar]3d64s2,故答案为:[Ar]3d64s2;(2)CO分子中C原子上有一对孤对电子,C、O原子都符合8电子稳定结构,则CO的结构式为C≡O,又等电子体中原子数和价电子数都相同,则N2、CN-、CO的原子数都是2,价电子数都是10,则互为等电子体,其中分子为:N2;CO分子的电子式为![]() ;(3)判断原子采取杂化方式时,先根据价层电子对互斥理论判断价层电子对,然后再确定采取的杂化方式.价层电子对数=σ键电子对数+中心原子上的孤电子对数,σ键电子对数=σ键个数=中心原子结合的原子个数,中心原子上的孤电子对数=(a-xb)/2,说明:对于分子,a为中心原子的价电子数,x为配位原子个数,b为配位原子最多能接受的电子数.在CH4中价层电子对数=σ键电子对数(4)+中心原子上的孤电子对数(0),所以碳原子采取sp3杂化.
;(3)判断原子采取杂化方式时,先根据价层电子对互斥理论判断价层电子对,然后再确定采取的杂化方式.价层电子对数=σ键电子对数+中心原子上的孤电子对数,σ键电子对数=σ键个数=中心原子结合的原子个数,中心原子上的孤电子对数=(a-xb)/2,说明:对于分子,a为中心原子的价电子数,x为配位原子个数,b为配位原子最多能接受的电子数.在CH4中价层电子对数=σ键电子对数(4)+中心原子上的孤电子对数(0),所以碳原子采取sp3杂化.
在CO分子中价层电子对数=σ键电子对数(1)+中心原子上的孤电子对数(1),所以碳原子采取sp杂化.CH3OH中,价层电子对数=σ键电子对数(4)+中心原子上的孤电子对数(0),所以碳原子采取sp3杂化; CH3OH分子之间有极性,CH3OH形成分子间氢键,沸点升高。


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
【题目】目前, 我市电能的主要来源是火力发电。 下列关于火力发电过程中能量转化关系的描述,正确的是
A. 化学能转化成机械能再转化成电能
B. 化学能转化成热能再转化成电能
C. 化学能转化成机械能再转化成热能再到机械能
D. 化学能转化成热能再转化成机械能再到电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的数值,下列叙述正确的是
A. a g C2H4和C3H6的混合物所含原子总数为![]()
B. 常温常压下,14 g由N2与CO组成的混合气体含有的原子数目为NA
C. 标准状况下,22.4 L H2O含有的分子数为 NA
D. 物质的量浓度为0.5 mol·L1的MgCl2溶液中,含有Cl个数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂的工业废水中含有大量的FeSO4 、较多的Cu2+和少量的Na+。为了减少污染并变废为宝,工厂计划从该废水回收硫酸亚铁和金属铜。请根据流程图,回答下列问题:

(1)物质X的化学式为________,操作1的名称:________
(2)写出A中主要成分的化学式:_____,在A中加入Y的离子方程式为:__________________
(3)工业废水中加入X所发生的离子方程式为:__________________________________;是否氧化还原反应____________(填“是”或“否”),如果是氧化还原反应,发生还原反应的是:______________(若非氧化还原反应则说明理由)。
(4)操作中的操作3是:___________、冷却结晶、过滤、洗涤、烘干。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用足量镁粉与一定量的某浓度的盐酸反应来制得氢气。由于反应速率太快,不易操作。为减慢反应速率,同时又不影响生成H2的总量,可向盐酸中加入的物质是
A.CH3COONa固体 B.NaOH溶液 C.(NH4)2SO4粉末 D.K2SO4固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)氨的水溶液显弱碱性,其原因为___________________(用离子方程式表示), 0.1 molL-1的氨水中加入少量的NH4Cl固体,溶液的pH________(填“升高”或“降低”);若加入少量的明矾,溶液中的NH4+的浓度__________(填“增大”或“减小”);
(2)25℃,两种酸的电离平衡常数如下表。
Ka1 | Ka2 | |
H2SO3 | 1.3×10-2 | 6.3×10-8 |
H2CO3 | 4.2×10-7 | 5.6×10-11 |
①HSO3-的电离平衡常数表达式K=___________________;
②0.10molL-1Na2SO3溶液中离子浓度由大到小的顺序为___________________;
③H2SO3溶液和NaHCO3溶液反应的离子方程式为___________________;
(3)银是一种贵金属,古代常用于制造钱币及装饰器皿,现代在电池和照明器材等领域亦有广泛应用。已知Ksp(AgCl)=1.8×10-10,若向5mL0.018molL-1的AgNO3溶液中加入5mL0.020molL-1的盐酸,混合后溶液中的Ag+的浓度为______molL-1,pH为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向密闭容器中充入物质A和B,发生反应aA(g)+bB(g)![]() cC(g)。反应过程中,物质A的体积分数
cC(g)。反应过程中,物质A的体积分数
和C的体积分数随温度(T)的变化曲线如图所示。下列说法正确的是
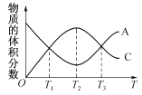
A.该反应在T1、T3温度时达到化学平衡 B.该反应在T2温度时达到化学平衡
C.该反应的逆反应是放热反应 D.升高温度,平衡会向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机高分子合成材料的出现是材料发展史上的一次重大突破,下列属于有机高分子合成材料的一组是( )
①家用保鲜袋 ②不锈钢 ③淀粉 ④尼龙布 ⑤汽车轮胎
A.①④⑤B.②③④C.②③⑤D.只有①⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com