
| A����һ����Ӧ�����ӷ���ʽΪClO-+2I-+2H+�TI2+Cl-+H2O |
| B������KI��Һ��������ΪI-������ΪI2��������I2����ɫ |
| C����ɫ����ʧ��ԭ����Na2SO3��Һ����Ư���� |
| D��������������ǿ������˳����ClO-��I2��SO42- |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
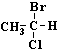 ��
��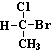 �����Ѻ��Ҵ�������ͼ�������ܵ��ۺ���ά�آݱ��״��ͼ�����
�����Ѻ��Ҵ�������ͼ�������ܵ��ۺ���ά�آݱ��״��ͼ�����| A���٢ڢܢ� | B���ڢܢޢ� |
| C���ۢݢޢ� | D���٢ܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ϡ���ᡢϡ������ܽ�ľ̿�����ɶ�����̼ |
| B��Na2O2��ˮ��Ӧ�����ȵ�Fe��ˮ������Ӧ�������ɼ� |
| C��Na��C��������Ӧ��ֻ����һ����Ӧ������ |
| D��NaHCO3����NH4��2CO3�������Ⱥ������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Ba2+��H+��Cl-��SO42- |
| B��K+��Ca2+��NO3-��CO32- |
| C��HCO3-��Na+��H+��NO3- |
| D��Na+��K+��CO32-��NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��KclO3��SO3����ˮ����Һ���ܵ��磬��KClO3��SO3��Ϊ����� |
| B����ˮ�м�������NH4Cl���壬pH���� |
| C����NaAlO2��Һ�еμ�NaHCO3��Һ���г������������� |
| D��AgCl��ת��ΪAgl����������ΪKsp��Agl����Ksp��AgCl�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����0.1 mol?L-1����ͭ��Һ�м���ZnS��ZnS��s��+Cu2+��aq��=CuS��s��+Zn2+��aq�� |
| B��������Ͷ������ͭ��Һ�У�2Na+Cu2+=2Na++Cu |
| C��������ʯ��������У�CaCO3+2H+=Ca2++H2O+CO2�� |
| D����Ba��OH��2��Һ�еμ�NaHSO4��Һ�����ԣ�Ba2++OH-+H++SO42-=BaSO4��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CuO����ԭ�� |
| B��CuO�������� |
| C��ͭԪ�ػ��ϼ۽��� |
| D��ͭԪ�ػ��ϼ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��10 mL��������Ϊ98%��H2SO4����ˮϡ����100 mL��H2SO4����������Ϊ9.8% |
| B��1molFe�������ϡHNO3��Ӧ��ת�Ƶĵ�����Ϊ2 NA |
| C����״���£�������ΪNA��CO��C2H4����������ԼΪ22.4 L������Ϊ28 g |
| D��һ���¶��£�l L 0.50 mol?L-1NH4C1��Һ��2 L0.25mol?L-1NH4C1��ҺNH4+����������Ϊ0.5NA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com