
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源:不详 题型:实验题
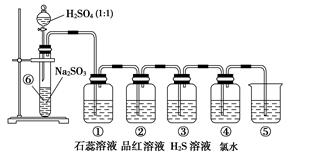
| 装置 | 实验现象 | 体现SO2的性质 |
| ① | | |
| ② | | |
| ③ | | |
| ④ | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
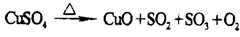
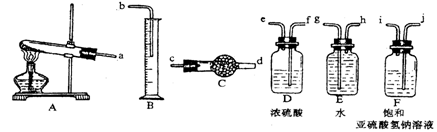
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
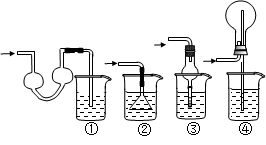
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用1mol的醋酸溶液和1.01mol的氢氧化钠溶液做中和热实验测得中和热的数值为57.3KJ/mol |
| B.通过实验得知在常温常压下,12g固体C和32g气体O2所具有的总能量一定大于44g气体CO2所具有的总能量 |
| C.室温下,用广泛pH试纸测得某溶液的pH为2.3 |
| D.用25mL滴定管做中和滴定时,用去某浓度的碱溶液21.7mL |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 编号 | 实验内容 | 实验目的 |
| A | 在Na2SO3溶液中加入HNO3酸化的Ba(NO3)2 ,产生白色沉淀 | 检验Na2SO3是否变质 |
| B | 将某气体通入品红溶液中,品红褪色 | 证明该气体是SO2 |
| C | 用洁净的玻璃棒蘸取NaOH溶液,点在湿润的pH试纸上,与标准比色卡对照 | 测定NaOH溶液的pH |
| D | 在两支试管中各加入4 mL 0.01 mol/L的KMnO4 酸性溶液,再分别加入0.1 mol/L H2C2O4 溶液2 mL、0.2 mol/L H2C2O4 溶液2 mL, 分别记录溶液褪色所需时间 | 探究相同条件下,溶液浓度对反应速率的影响 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
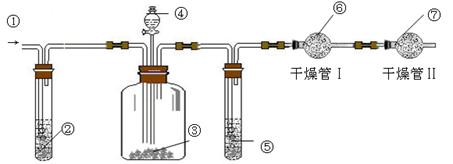
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
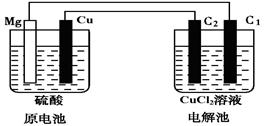
| A.从镁电极经导线流向C1极 | B.从C1极经导线流向镁电极 |
| C.从铜电极经导线流向C2极 | D.从C2极经导线流向铜电极 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com