
| A. | 氯水 | B. | 液氨 | C. | 氨水 | D. | 漂白粉 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
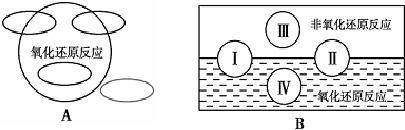
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,A或B可以与水发生反应 | |
| B. | A与B用导线连接插入稀HNO3中,则形成原电池且B极上有H2放出 | |
| C. | A与B用导线连接插入B(NO3)2中,B极发生的电极反应式可能为:B2++2e-═B | |
| D. | 电解A(NO3)2与B(NO3)2的混合液,在阳极先析出B(使用碳电极) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 我国“西气东输”中的“气”指的是石油气 | |
| B. | 废弃物在一定条件下发生化学反应,产生热值较高的可燃性气体,该过程属于生物化学转化 | |
| C. | 煤干馏的主要产物为焦炭、煤焦油、粗氨水和焦炉气 | |
| D. | 石油分馏是化学变化,可得到汽油、煤油等产品 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液中所含的离子是:Fe2+?Na+?SO42-?NO3-? | |
| B. | 若向该溶液中加入过量的稀硫酸,产生的气体在空气中能变成红棕色 | |
| C. | 若向该溶液中加入过量的稀硫酸和KSCN溶液,溶液显血红色 | |
| D. | 若向该溶液中加入足量的NaOH 溶液,充分反应后,过滤?洗涤?灼烧,最终所得固体的质量为72g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作 | 实验目的 | |
| A | 向甲酸钠溶液中加新制的Cu(OH)2并加热 | 确定甲酸钠具有醛基性质 |
| B | 蛋白质水溶液中滴入CuSO4溶液 | 验证蛋白质的盐析 |
| C | 向淀粉溶液中加入3~5mL稀硫酸,加热煮沸后冷却,再加入银氨溶液,水浴加热 | 验证淀粉是否水解 |
| D | 将氯乙烷与氢氧化钠溶液共热一段时间,再向冷却后的混合液中滴加硝酸银溶液 | 检验水解产物中的氯离子 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
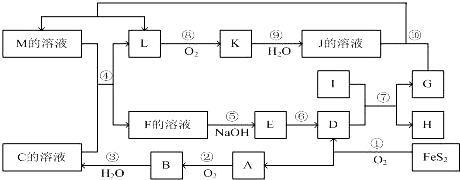
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CuFeS2中被氧化和被还原的原子数之比为2:1 | |
| B. | 该反应中有两种物质作氧化剂 | |
| C. | 每生成1mol SO2,反应中转移6mol电子 | |
| D. | C uFeS2中只有硫元素被氧化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com