
 氨是最重要的化工产品之一.
氨是最重要的化工产品之一.| 弱电解质 | H2CO3 | NH3•H2O |
| 电离平衡常数 | Ka1=4.30×10-7 | 1.77×10-5 |
| Ka2=5.61×10-11 |
分析 (1)在一个一定容积的密闭容器中加入1mol 氮气和3mol 氢气,在一定条件下发生反应合成氨气,当反应物转化率达10%时,反应的氮气为0.1mol,测得放出的热量为9.24kJ,则反应1molN2放热92.4KJ,结合热化学方程式书写方法,标注物质聚集状态和对应反应焓变写出;
(2)[Cu(NH3)2CH3COO](l)+CO(g)+NH3(g)?[Cu(NH3)3]CH3COO•CO(l)△H<0,反应为气体体积减小的放热反应,提高CO的吸收效率需要平衡正向进行,结合化学平衡移动原理和平衡移动方向分析判断需要的条件
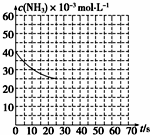
(3)依据化学方程式和平衡常数K=$\frac{c({H}_{2}O)}{c(C{O}_{2}){c}^{2}(N{H}_{3})}$,结合化学平衡三段式列式计算平衡浓度,计算平衡常数;依据催化剂的作用画出图象,曲线的转折点在横坐标40之前,纵坐标必需在20的线上;
(4)①依据弱电解质电离平衡常数比较弱电解质强弱,盐类水解原理分析判断溶液酸碱性;
②依据溶液中离子性质,电荷守恒、物料守恒、离子浓度大小比较的方法分析选择.
解答 解:(1)在一个一定容积的密闭容器中加入1mol 氮气和3mol 氢气,在一定条件下发生反应合成氨气,当反应物转化率达10%时,反应的氮气为0.1mol,测得放出的热量为9.24kJ,则反应1molN2放热92.4KJ,反应的热化学方程式为:N2(g)+3H2( g)═2NH3(g)△H=-92.4 kJ•mol-1,
故答案为:N2(g)+3H2( g)═2NH3(g)△H=-92.4 kJ•mol-1;
(2)[Cu(NH3)2CH3COO](l)+CO(g)+NH3(g)?[Cu(NH3)3]CH3COO•CO(l)△H<0,反应为气体体积减小的放热反应,提高CO的吸收效率需要平衡正向进行,
A.高压平衡正向进行,增大CO吸收率,故A正确;
B.反应为放热反应,高温平衡逆向进行,CO吸收率减小,故B错误;
C.把[Cu(NH3)3]CH3COO•CO分离出去对气体吸收影响不大,故C错误;
D.增大CO浓度平衡正向进行,但会减小CO的吸收率,故D错误;
吸收CO后的乙酸铜氨液经过适当处理后又可再生,恢复其吸收CO的能力以供循环使用,依据化学平衡[Cu(NH3)2CH3COO](l)+CO(g)+NH3(g)?[Cu(NH3)3]CH3COO•CO(l);△H<0,反应是气体体积减小的放热反应,平衡逆向进行是再生的原理,再生的适宜条件是高温低压,
故答案为:A;B;
(3)2NH3(g)+CO2(g)?CO(NH2)2(l)+H2O(g),反应进行到40s时达到平衡,反应达到平衡时CO2的转化率为50%,消耗二氧化碳浓度0.02mol/L×50%=0.01mol/mol;
2NH3(g)+CO2(g)?CO(NH2)2(l)+H2O(g)
起始量(mol/L) 0.04 0.02 0 0
变化量(mol/L) 0.02 0.01 0 0.01
平衡量(mol/L) 0.02 0.01 0 0.01
K=$\frac{c({H}_{2}O)}{c(C{O}_{2}){c}^{2}(N{H}_{3})}$=$\frac{0.01}{0.0{2}^{2}×0.01}$=2500
若反应延续至70s,保持其它条件不变情况下,使用催化剂时,改变反应速率,不改变化学平衡,曲线的转折点在横坐标40之前,纵坐标必需在20的线上,该反应的进程曲线为如图所示:曲线的转折点在横坐标40之前,纵坐标必需在20的线上, ,
,
故答案为:2500; ;
;
(4)①分析电离平衡常数可知电离程度,NH3•H2O>H2CO3>HCO3-,对应盐水解程度NH4+<HCO3-<CO32-,常温下0.1mol•L-1的(NH4)2CO3溶液呈碱性,由于NH3•H2O的电离平衡常数大于HCO3-的电离平衡常数,因此CO32-水解程度大于NH4+水解程度,溶液中c (OH-)>c(H+),溶液呈碱性;
故答案为:碱,由于NH3•H2O的电离平衡常数大于HCO3-的电离平衡常数,因此CO32-水解程度大于NH4+水解程度,溶液中c (OH-)>c(H+),溶液呈碱性;
②A.溶液中铵根离子浓度大于碳酸根离子浓度,碳酸根离子水解程度大于铵根离子水解程度,所以溶液中离子浓度大小为:c(NH4+)>c(CO32-)>c(HCO3-)>c(NH3•H2O),故A正确;
B.溶液中存在电荷守恒为:c(NH4+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-),故B错误;
C.依据溶液中物料守恒得到:c(CO32-)+c(HCO3-)+c(H2CO3)=0.1mol•L-1 ,故C正确;
D.依据溶液中物料守恒,n(N):n(C)=2:1,结合溶液中离子种类和守恒关系得到:c(NH4+)+c(NH3•H2O)=2c(CO32-)+2c(HCO3-)+2c(H2CO3),故D正确;
故答案为:B.
点评 本题考查了热化学方程式书写方法,化学平衡影响因素分析,电解质溶液中离子浓度关系的应用判断,掌握基础是关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 冰熔化时只破坏范德华力而不破坏共价键 | |
| B. | 对于分子,其范德华力只随着相对分子质量的增大而增大 | |
| C. | NH3极易溶于水而CH4难溶于水的原因只是NH3是极性分子,CH4是非极性分子 | |
| D. | 氢键存在于分子之间,也存在于分子之内 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca2+Mg2+ CO32-Cl- | B. | Fe3+Cl- Na+H+ | ||
| C. | H+ Ag+ NO3- NH4+ | D. | CO32-H+Na+OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
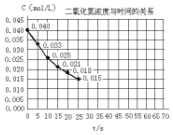 二氧化氮在加热条件下能够分解成一氧化氮和氧气.该反应进行到45秒时,达到平衡(NO2浓度约为0.0125mol/L).图中的曲线表示二氧化氮分解反应在前25秒内的反应进程.
二氧化氮在加热条件下能够分解成一氧化氮和氧气.该反应进行到45秒时,达到平衡(NO2浓度约为0.0125mol/L).图中的曲线表示二氧化氮分解反应在前25秒内的反应进程.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.8molNaCl所含离子数 | B. | 标准状况下5.6L CO2所含原子数 | ||
| C. | 1L1 mol•L-1盐酸溶液所含H原子数 | D. | 10g氖气所含原子数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com