
| A、2.4克金属镁变成镁离子时失去的电子数目为0.1NA(NA代表阿伏加德罗常数) |
| B、40g NaOH溶解于500mL水中,所得溶液的物质的量浓度为2mol?L-1 |
| C、1mol H2的质量是2g?mol-1 |
| D、等物质的量的O3和H2O中所含的原子个数相等 |
| 2.4g |
| 24g/mol |
| 40g |
| 40g/mol |


 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
| A、18gD2O中含有质子的数目为NA |
| B、标准状况下,11.2L甲烷和乙烯的混合物所含氢原子的数目为2NA |
| C、1L0.1mol?L-1CH3COOH溶液中含有分子的数目小于0.1NA |
| D、1L0.5 mol?L-1Na2CO3溶液中含有CO32-的数目为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=3的溶液:Ca2+、CH3COOH、Br-、Na+ |
| B、水电离的c(H+)=1×10-13mo1?L-1的溶液:Na+、K+、SO42-、CO32- |
| C、含有大量Fe3+的溶液:Na+、Mg2+、NO3-、SCN- |
| D、含有大量NO3-的溶液:NH4+、H+、SO42-、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 此装置:可用来证明碳的非金属性比硅强 |
B、 此装置:橡皮管的作用是平衡压强,使水顺利流下 |
C、 此装置:用图示的方法能检查此装置的气密性 |
D、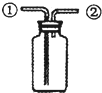 此装置:可收集二氧化碳或氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com