
【题目】下列反应中,不属于氧化还原反应的是( )
A.H2+Cl2=2HCl
B.2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
C.NH4HCO3![]() NH3↑+CO2↑+H2O
NH3↑+CO2↑+H2O
D.Zn+H2SO4=H2↑+ZnSO4
科目:高中化学 来源: 题型:
【题目】乙醇(C2H5OH)是生活中常见的物质,下图给出了乙醇的结构式和球棍模型。

I.乙醇燃料电池(DEFC)具有很多优点,引起了人们的研究兴趣。现有以下三种乙醇燃料电池。
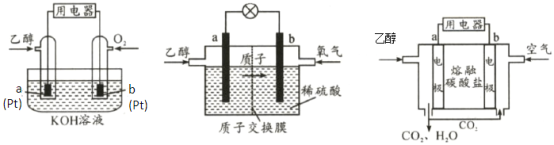
碱性乙醇燃料电池 酸性乙醇燃料电池 熔融盐乙醇燃料电池
(1)三种乙醇燃料电池中正极反应物均为_______。(填化学式)
(2)碱性乙醇燃料电池中,电极a上发生的电极反应式为_______,使用空气代替氧气,电池工作过程中碱性会不断下降,其原因是_______。
(3)酸性乙醇燃料电池中,电极b上发生的电极反应式为_______。
(4)熔融盐乙醇燃料电池中若选择熔融碳酸钾为介质,电池工作时,CO32-向电极_______(填“a”或“b”)移动。
II. 已知气相直接水合法可以制取乙醇:H2O(g)+C2H4(g)![]() CH3CH2OH(g)。当n(H2O):n(C2H4)=1:1时,乙烯的平衡转化率与温度、压强的关系如下图:
CH3CH2OH(g)。当n(H2O):n(C2H4)=1:1时,乙烯的平衡转化率与温度、压强的关系如下图:
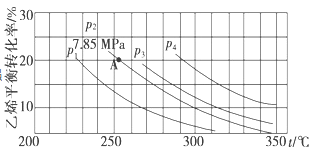
(1)图中压强p1、p2、p3、p4的大小顺序为:_______,理由是:_______。
(2)气相直接水合法采用的工艺条件为:磷酸/硅藻土为催化剂,反应温度290℃,压强6.9 MPa,n(H2O):n(C2H4)=0.6:1。该条件下乙烯的转化率为5%。若要进一步提高乙烯的转化率,除了可以适当改变反应温度和压强外,还可以采取的措施有_______、_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化工生产是指对原料进行化学加工,最终获得有价值的产品的生产过程。某研究小组利用含硫酸亚铁和硫酸铜的工业废料制备铁红(氧化铁)和硫酸铵晶体。流程如图:
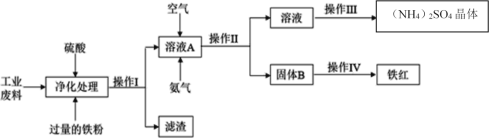
请回答下列问题:
(1)操作I的名称_____,操作Ⅲ的名称____。
(2)滤渣的成分为_____。
(3)请写出溶液A中反应的离子方程式___。在标准状况下,转移0.4NA个电子时,通入的空气体积为_____。
(4)测定废料中硫酸铜的质量分数:称取ag废料样品,将操作I得到的滤渣用足量的稀硫酸溶解、过滤、洗涤、干燥,称得固体的质量为b g,则废料中硫酸铜的质量分数____(写出表达式)。
(5)向工业废料溶液中加入足量的酸性高锰酸钾,写出有关的离子方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法正确的是( )
A. 乙醇和丙三醇互为同系物
B. 环己烯(![]() )分子中的所有碳原子共面
)分子中的所有碳原子共面
C. 分子式为C5H10O2,且属于羧酸的同分异构体共有9种(不考虑立体异构)
D. 二环己烷( ![]() )的二氯代物有7种结构(不考虑立体异构)
)的二氯代物有7种结构(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D 四种化合物,分别由K+ 、Ba2+ 、SO42 、CO32、OH中的两种组成,它们具有下列性质:①A不溶于水和盐酸;②B不溶于水,但溶于盐酸,并放出无色无刺激性气味的气体E;③C的水溶液呈碱性,与硫酸反应生成A;④D可溶于水,与硫酸作用时放出气体E,E可使澄清石灰水变浑浊。
(1)推断A、B、C、D的化学式:
A____________;B____________;C_____________;D____________。
(2)写出下列反应的离子方程式:
C与盐酸反应___________________________________________________
B与盐酸反应_______________________________________________________
过量的E与澄清石灰水反应___________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里需240mL0.1mol/L的CuSO4溶液。
(1)配制该溶液因选__mL容量瓶,以下配制方法正确的是__(填字母)。
A.称取3.84gCuSO4溶于盛有250mL水的烧杯中
B.称取6.0g胆矾溶于盛有250mL水的烧杯中
C.称取4.0gCuSO4溶于盛有250mL水的烧杯中
D.称取6.25g胆矾配成250mL溶液
(2)假如其它操作均正确无误,分析下列情况对配制溶液浓度的影响(填“偏高”“偏低”“不变”)
A.定容时俯视观察刻度线:___;
B.移液时,对于溶解CuSO4(或胆矾)的烧杯没有洗涤:___;
C.定容后,将容量瓶振荡摇匀,静置时发现液面低于刻度线,又补加水至刻度线:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G各物质间的关系如下图所示,其中B、D为气体单质。则下列说法错误的是

A.已知C的浓溶液在催化剂存在的条件下加热,能与B反应生成D,由此可以推断B的氧化性比MnO2强
B.反应②的离子方程式为![]()
C.新配制的F溶液一般需要加入铁屑和稀盐酸,前者用于防止Fe2+被空气氧化成Fe3+,后者可抑制Fe2+的水解
D.若反应①在常温下进行,则1molA在反应中能转移1mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃、101 kPa时,强酸与强碱的稀溶液中发生中和反应的中和热为57.3 kJ·mol-1,则下列描述正确的是
A. KOH(aq)+![]() H2SO4(aq)===
H2SO4(aq)===![]() K2SO4(aq)+H2O(1) ΔH=-57.3 kJ·mol-1
K2SO4(aq)+H2O(1) ΔH=-57.3 kJ·mol-1
B. NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(1) ΔH=+57.3 kJ·mol-1
C. H2SO4和Ca(OH)2反应的中和热为ΔH=2×(-57.3) kJ·mol-1
D. 稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂。请填写下列空白。
(1)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视_______,直到因加入一滴盐酸后,溶液由________色变为________色,并________为止。
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是__________。
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
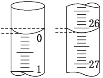
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则起始读数为_______mL,终点读数为_______mL,所用盐酸溶液的体积为_______mL。
(4)某学生根据3次实验分别记录有关数据如下表:
滴定 次数 | 待测NaOH溶液的体积/mL | 0.100 0 mol·L-1 盐酸的体积/mL | ||
滴定前读数 | 滴定后读数 | 溶液体积/mL | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
依据上表数据列式计算该NaOH溶液的物质的量浓度__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com