
下列关于氧化还原反应的说法,正确的是
| A.氧化还原反应的特征是电子的转移 |
| B.氧化剂在反应中被还原,生成氧化产物 |
| C.同一反应中,氧化剂得电子的总数一定等于还原剂失电子的总数 |
| D.任何反应中一定有氧化剂和还原剂,且氧化剂和还原剂可以为同种物质 |
科目:高中化学 来源: 题型:单选题
已知下列离子在酸性条件下都能氧化KI,它们自身发生如下变化:① Cr2O72-→ Cr3+,②IO3-→ I2,③MnO4-→ Mn2+。如果分别用等物质的量的这些离子氧化足量的KI,得到I2的物质的量由多到少的顺序正确的是
| A.②=③>① | B.①>②=③ | C.②>③>① | D.①=②>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
化学上,通常把有化合价变化的反应称作氧化还原反应,下列反应属于氧化还原反应的是( )
| A.CO2+H2O=H2CO3 |
B.2H2O2 2H2O+O2↑ 2H2O+O2↑ |
C.CaCO3 CO2↑+ CaO CO2↑+ CaO |
| D.CuSO4+2NaOH =Cu(OH)2↓+Na2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
氧化还原反应与四种基本反应类型的关系如下图所示,则下列化学反应属于区域3的是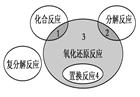
| A.4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
B.2KMnO4 K2MnO4+MnO2+O2↑ K2MnO4+MnO2+O2↑ |
C.4NH3+5O2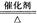 4NO+6H2O 4NO+6H2O |
| D.Fe+CuSO4=FeSO4+Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是
A.一定条件反应:2CO(g)  CO2(g)+C(s)可自发进行,则该反应的△H>0 CO2(g)+C(s)可自发进行,则该反应的△H>0 |
| B.向硫酸亚铁溶液中滴加硫氰化钾溶液产生血红色沉淀说明溶液已变质 |
| C.在反应KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O中,当生成1.5mol Cl2时,反应中转移的电子数为2.5NA |
| D.相同物质的量浓度的下列溶液:①NH4HSO4②NH4Cl③NH3·H2O,水电离程度由大到小的顺序是:①>②>③ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在5.6 g Fe粉中加入过量的稀硫酸溶液,待反应完全后,再加入1mol·L-1 KNO3溶液25mL,恰好反应完全。该反应的方程式为:
FeSO4 +KNO3 +H2SO4→K2SO4 +Fe2(SO4)3+NxOy + H2O(未配平),则对该反应的下列说法正确的是
| A.化学方程式中按物质顺序的计量数是:8、2、5、1、4、1、5 |
| B.反应中氧化产物是N2O |
| C.反应过程中转移的电子数为8mol电子 |
| D.氧化产物和还原产物的物质的量之比为4∶1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
常温下,往H2O2溶液中滴加少量FeSO4溶液,可发生如下两个反应:
2Fe2++H2O2+2H+=2Fe3++2H2O 2Fe3++H2O2=2Fe2++O2↑+2H+
下列说法不正确的是( )
| A.H2O2的氧化性比Fe3+强,其还原性比Fe2+弱 |
| B.在反应过程中,溶液的pH基本不变 |
| C.在反应过程中,Fe2+和Fe3+的总量保持不变 |
| D.H2O2生产过程要严格避免混入Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是( )。
A.根据反应Cu+H2SO4 CuSO4+H2↑可推出Cu的还原性比H2的强 CuSO4+H2↑可推出Cu的还原性比H2的强 |
| B.在反应CaH2+2H2O===Ca(OH)2+2H2↑中,水作氧化剂 |
| C.反应3NO2+H2O===2HNO3+NO中氧化剂和还原剂的物质的量之比是3∶1 |
| D.因Cl2的氧化性强于I2的氧化性,所以置换反应I2+2NaClO3===2NaIO3+Cl2不能发生 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com